编辑推荐:
2024年12月8日,中国科学院上海药物研究所张继稳团队联合临港实验室、西藏大学、山东则正医药技术有限公司、英国布拉德福德大学、沈阳药科大学、中国食品药品检定研究院、中国科学院上海高等研究院等,在Journal of Controlled Release上发表了题为“3D channel maze” to control drug release from multiple unit tablets(控制多单元片药物释放的“3D通道迷宫”机制)的研究论文
2024年12月8日,中国科学院上海药物研究所张继稳团队联合临港实验室、西藏大学、山东则正医药技术有限公司、英国布拉德福德大学、沈阳药科大学、中国食品药品检定研究院、中国科学院上海高等研究院等,在Journal of Controlled Release上发表了题为“3D channel maze” to control drug release from multiple unit tablets(控制多单元片药物释放的“3D通道迷宫”机制)的研究论文。

缓控释给药系统因其能够提供可控、可预测的药物释放速率,一直是药物递送领域的研究热点。药物的缓释、控释涉及多种机制,包括水分和药物的扩散、基质侵蚀、聚合物溶胀、渗透效应和离子交换等。其中,扩散是缓控释给药系统或传统剂型的基本机制。以扩散作用为主要释放机制的给药系统可分为两大类:储库型系统和基质型系统。以微丸压制缓释片为代表的多单元微丸给药系统是一种新型的缓控释给药系统,具有避免药物局部浓度过高、患者依从性高、副作用少等优点。从制剂3D结构出发,揭示药物释放过程和机制,对深入理解剂型,尤其是以微丸压制缓释片为代表的高端制剂的体外和体内行为至关重要。同步辐射显微计算机断层扫描(SR-μCT)等先进成像技术为制剂结构研究提供了强大的3D结构研究工具,本研究应用SR-μCT对茶碱微丸缓释片进行3D成像,探究了缓释片整体结构及单微丸在释药过程中的内部结构变化,并结合微丸缓释片整体和单微丸的释放动力学特征,提出了“3D通道迷宫”的药物缓控释放新机制(图1)。

图1 “3D通道迷宫”释放模型
SR-μCT能够清晰地展示茶碱微丸缓释片的内部结构(图2 A)。茶碱微丸在径向上随机分布,但是位于茶碱微丸缓释片背面的微丸数量多于正面。此外,径向和轴向切片均显示茶碱微丸缓释片主要由三个区域组成:茶碱单微丸、缓冲保护层(橙色区域)和基质层(黄色区域)(图2 B)。根据重建获得的3D图像,提取出茶碱微丸缓释片中单微丸的结构(图2 C)。单微丸由丸芯和包衣层组成,直径为 0.5 ~ 1.2 mm。包衣层相对均匀紧密、平均厚度约 100 μm。
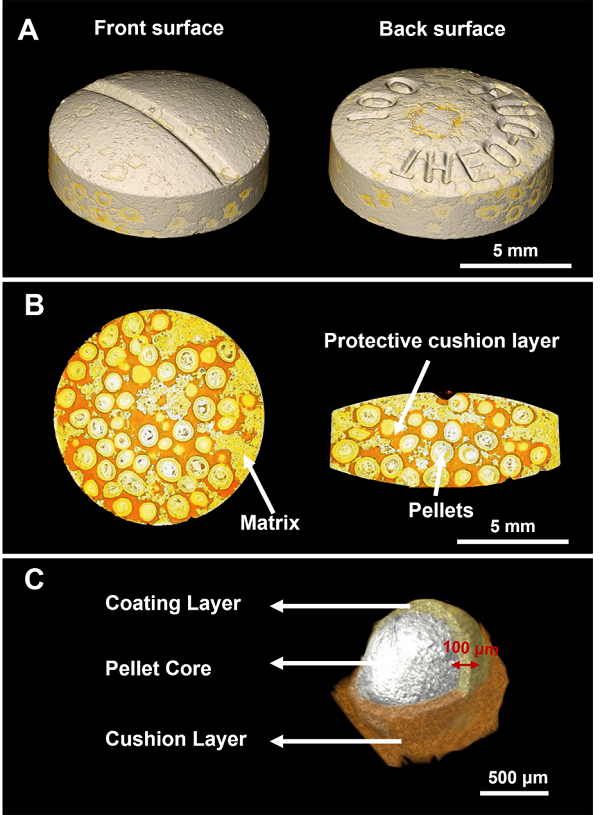
图2 茶碱微丸缓释片原位结构:(A)茶碱微丸缓释片的3D结构;(B)茶碱微丸缓释片的内部切片结构;(C)茶碱微丸缓释片内部微丸的3D结构
基质层和核心区域(缓冲保护层和茶碱微丸)在茶碱微丸缓释片的不同释放阶段起着主导作用(图3 A)。速释阶段(溶出初始阶段),药片外围的基质层(包括药物和可溶性辅料)迅速溶出,而核心区域基本保持不溶(图3 B);位于片剂边缘、缺乏缓冲保护材料保护的微丸发生溶解。控释阶段,在微丸被溶解的同时,出现细小的出口和通道,释放溶解的药物分子。然而,由于缓冲保护层的隔离作用(部分可溶解),溶解的药物分子缓慢通过曲折的孔隙通道被释放出来(图3 C)。在控释阶段,微丸之间的孔隙、通道连通,通道迂回曲折、错综复杂,形成“3D通道迷宫”结构。当药物分子溶解到液体介质中时,需从迷宫中找到出路。即使药物分子在同一时间从同一起点出发,一部分药物能快速找到出路,而另一部分则会被延迟,需消耗较长的时间走出迷宫。由于“3D通道迷宫”的延迟效应,药物从缓释片的核心区域逃逸所需的时间被区分开,最终形成控释效果。
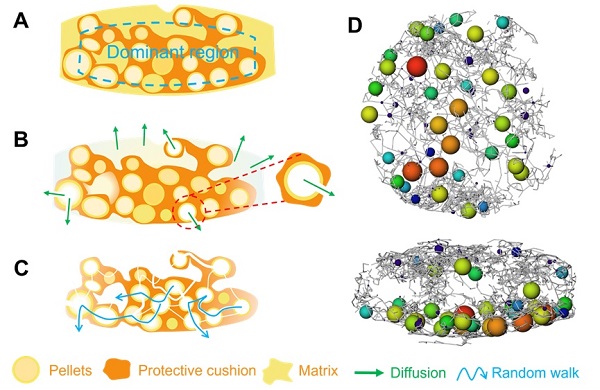
图3 “3D通道迷宫”释放模型:(A)茶碱微丸缓释片内部结构;(B)释放初始阶段:药物通过扩散作用进行释放;(C)缓控释阶段:药物通过“3D通道迷宫”模型进行释放;(D)茶碱微丸缓释片内的“3D通道迷宫”
“3D通道迷宫”机制为阐明茶碱微丸缓释片的缓控释放机制提供了一个新视角。与传统缓释给药系统的扩散机制不同,“3D通道迷宫”模型强调的是药片内部孔隙网络的门控作用。药物在孔隙网络中自由溶解和扩散,但由于药物还受到曲折复杂的通道网络的限制,不能被视为释放。只有当药物穿过3D通道网络的出口、并进入制剂外的介质时,才是真正意义上的的药物释放。“3D通道迷宫”中药物的释放受多个过程的制约:水的扩散、药物的溶解、药物在3D通道网络中的扩散以及药物从“3D通道迷宫”中逸出,迷宫的门控起着关键的控释作用。
上海药物所硕士研究生许慧鹏、张柳,西藏大学博士研究生方龙伟为本文共同第一作者。上海药物所张继稳研究员、伍丽副研究员与临港实验室殷宪振研究员为本论文的共同通讯作者。
全文链接:https://doi.org/10.1016/j.jconrel.2024.12.014
(供稿部门:张继稳课题组)
 生物通微信公众号
生物通微信公众号
生物通 版权所有