编辑推荐:
本研究针对现有磷酸肌醇(PIXPs)传感器在监测PI4P代谢动态中的局限性,开发了基于分裂GFP的新型传感器sGFP(PI4P)。通过比较传统的ddRFP(PI4P)传感器,研究人员证实sGFP(PI4P)具有高灵敏度、低表达干扰和多重检测优势,成功应用于OSBP抑制剂OSW-1和PI4K抑制剂IN10/PI273的药效评估,为研究PI4P在胆固醇转运和药物开发中的代谢调控提供了创新工具。
在细胞生物学领域,磷酸肌醇(PIXPs)如同分子世界的"货币",在不同细胞区室间流通并执行重要功能。其中磷脂酰肌醇-4-磷酸(PI4P)作为关键代谢中间体,既是PI(4,5)P2和PI(3,4)P2的前体,又在高尔基体介导的胆固醇反向运输中扮演核心角色。然而这个动态分子世界的观测工具却长期存在缺陷——现有基于FRET、BRET或ddRFP的传感器虽能捕捉快速信号转导,却难以监测代谢尺度上的PI4P变化,且高表达水平会干扰细胞正常功能。这种技术瓶颈严重制约了人们对PI4P在慢性病理过程(如胆固醇代谢紊乱)和长期药物处理中作用机制的理解。
为突破这一限制,Samantha K. A. Manuel等研究团队在《Scientific Reports》发表的研究中,创新性地将分裂GFP(sGFP)技术应用于代谢物传感领域。研究人员设计了两类PI4P传感器:沿用传统思路的ddRFP(PI4P)和首创的sGFP(PI4P),均采用FAPP1的PH结构域作为靶向模块。通过系统比较发现,虽然ddRFP(PI4P)在分钟级响应上表现优异,但sGFP(PI4P)在稳定表达条件下展现出56倍的信号强度优势,且能在极低表达水平下维持功能,显著降低了对细胞行为的干扰。这种性能差异源于两种传感器的不同工作原理:ddRFP依赖瞬时相互作用产生信号,而sGFP通过PI4P介导的片段互补形成稳定荧光结构,具有"慢开-慢关"的独特动力学特征。
研究采用的主要技术方法包括:基于FAPP1-PH结构域的传感器分子设计、稳定转染细胞系的构建与筛选、时间分辨荧光显微成像分析、流式细胞术定量检测、细胞裂解液荧光测定等。通过OSW-1处理模型验证传感器性能,该化合物通过抑制氧固醇结合蛋白(OSBP)阻断PI4P/胆固醇反向运输,导致PI4P在高尔基体积累。
研究结果部分显示:
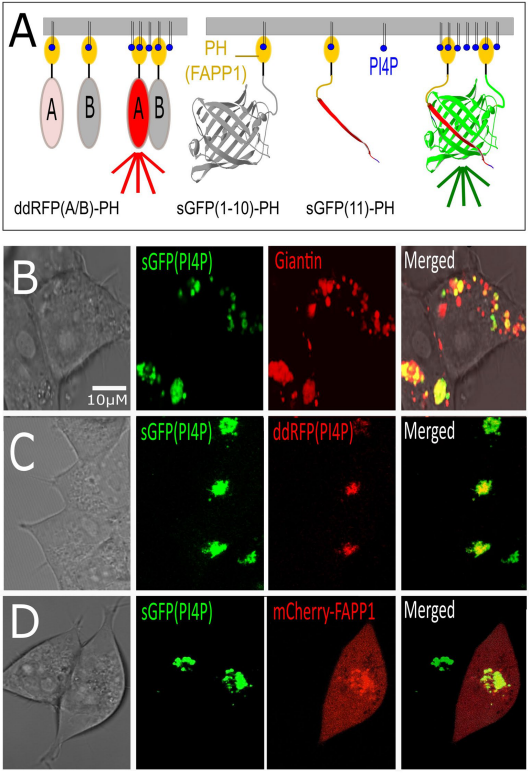
"sGFP(PI4P)传感器功能与特异性"证实该传感器信号主要定位于高尔基体区,与Giantin标记区域重叠,且与经典探针mCherry-FAPP1共定位。值得注意的是,sGFP(PI4P)显著降低了传统探针存在的游离背景信号问题。
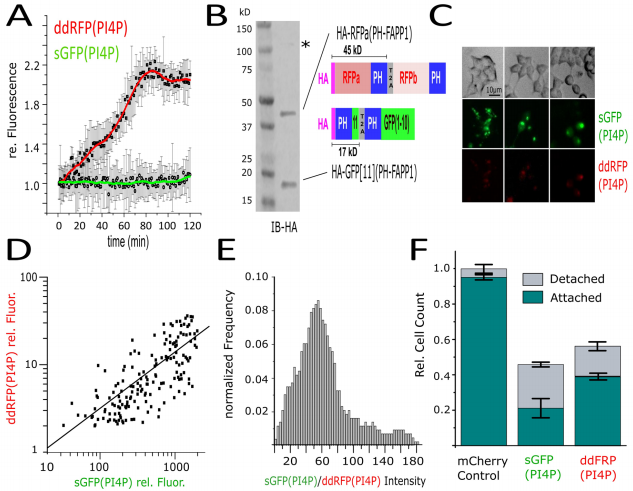
"ddRFP传感器更动态但sGFP传感器信号更强"揭示了两类传感器的核心差异:在OSW-1处理的实时监测中,ddRFP能在2小时内响应PI4P升高,而sGFP由于需要荧光蛋白成熟过程而表现滞后。但在信号强度方面,sGFP展现出56倍的优势,使其能在生理相关低表达水平下工作。
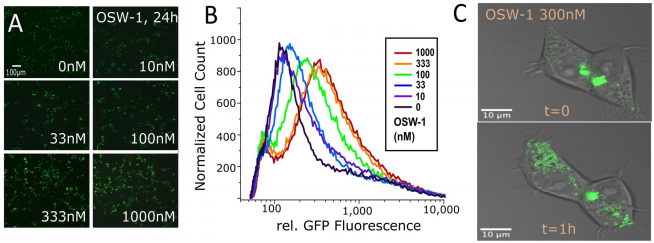
"sGFP(PI4P)稳定表达的检测优势"展示了该传感器在实际应用中的多重价值:不仅能通过流式细胞术定量OSW-1剂量效应,还能清晰显示药物诱导的高尔基体结构紊乱,同时保持低背景干扰。
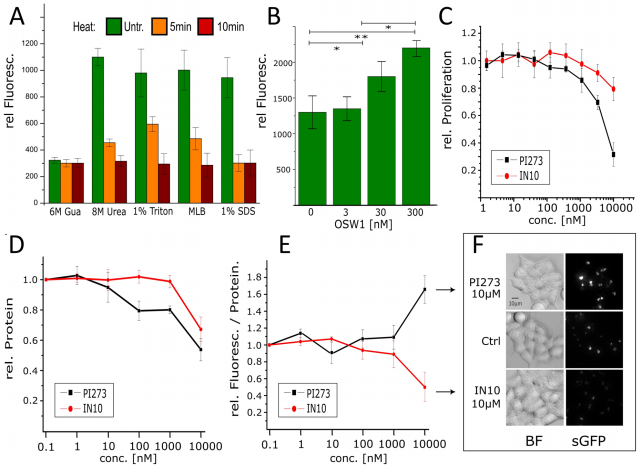
"细胞裂解液检测可行性"创新性地证实sGFP信号在8M尿素裂解条件下保持稳定,为高通量筛选奠定基础。应用该技术评估PI4KB抑制剂IN10和PI4K2A抑制剂PI273时,发现前者剂量依赖性地降低PI4P水平,后者却在抑制增殖的同时意外引起PI4P积累,提示其对高尔基体PI4P利用的次级影响。
这项研究的结论部分强调了sGFP(PI4P)传感器的多重创新价值:作为首个应用于代谢物检测的分裂荧光蛋白传感器,其低表达需求、多重检测兼容性(显微、流式、裂解液)和生物学中性特点,完美弥补了现有技术在代谢研究中的不足。特别是在药物开发领域,该传感器成功揭示了PI273双重作用的意外发现——在抑制PI4K2A降低增殖的同时,通过未知机制引起高尔基体PI4P积累,这种复杂调控关系是传统细胞外试验无法发现的。研究还提出了传感器优化方向,如采用嗜肺军团菌SidM的P4M结构域可能扩展检测范围,以及利用新型快速互补sGFP变体改善响应速度。
这项工作的更深远意义在于为磷酸肌醇代谢研究提供了全新范式。PI4P作为连接快速信号传导与慢性代谢调节的关键节点,其动态平衡紊乱与动脉粥样硬化、神经退行性疾病等多种病理过程相关。sGFP(PI4P)传感器的出现,使科学家首次能在生理相关表达水平下,长期监测PI4P在胆固醇稳态、膜运输障碍等慢过程中的变化,为相关疾病机制研究和药物开发开辟了新途径。该技术路线还可能启发更多代谢物传感器的设计,推动细胞代谢研究的革新。
生物通 版权所有