编辑推荐:
科学家开发了一种模块化的、基于多价纳米体的平台,具有增强的适应性多表位靶向性,以解决快速进化的病毒(如SARS-CoV-2)突变和逃避现有治疗的能力。
病毒和细菌等病原体通常具有高度的遗传多样性,并且具有产生逃逸突变的能力,这些突变会破坏宿主免疫力和治疗方法的有效性。自COVID-19大流行开始以来,SARS-CoV-2迅速变异,疫苗和治疗方法难以跟上病毒的快速进化,使许多疫苗和治疗方法的效果降低。大多数治疗性抗体针对单个病毒位点,并在一年内随着新变异的出现而失效。解决这些逃逸机制需要针对进化上保守的脆弱区域,因为这些区域的突变通常会带来适应性成本——持久对策的发展需要针对多个中和表位,最理想的是进化保守的表位。
纳米体(Nbs)已经成为抗病毒治疗的一种很有前途的解决方案。亲和力成熟的纳米体可以特异性地结合多种中和表位,包括保守的、和神秘的位点,利用不同的机制来阻止病毒感染。
基于此,西奈山伊坎医学院的一个研究小组领导的科学家们开发了一种基于抗体的平台:适应性多表位靶向增强亲和力(AMETA)—— 一个模块化的多价纳米体平台,能够将有效的双特异性纳米体结合到人类免疫球蛋白M (IgM)支架上——IgM本身是免疫系统帮助抵抗感染的自然防御的一部分,AMETA可以展示20多个多靶向纳米体,能够与多个保守和中和的表位实现超强结合,显著提高了与病毒结合的能力。因此,AMETA在对抗高级变异方面要有效得多,其效力是传统抗体的一百万倍,而传统抗体只针对单一靶点。研究结果新发表在《Cell》上。
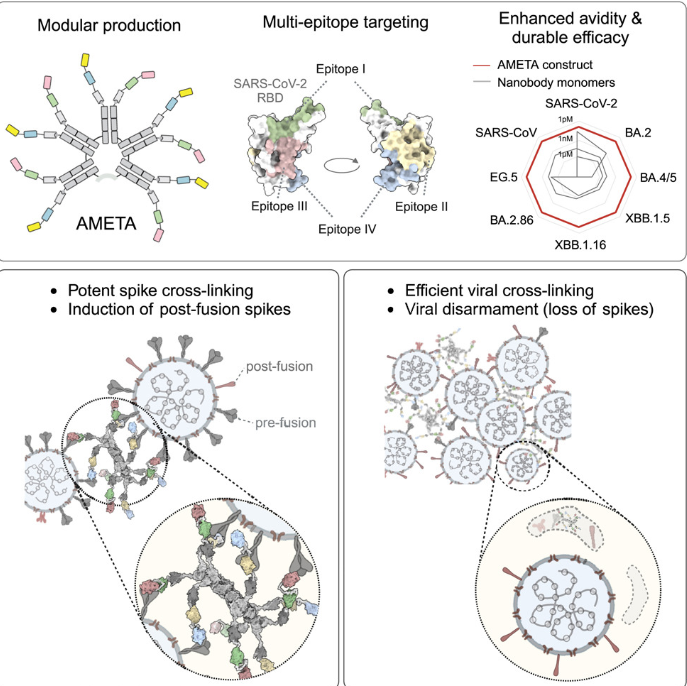
AMETA是一种模块化的多价平台,它使用工程纳米体(Nbs)同时靶向病毒的多个稳定区域。该技术将有效的双特异性纳米体与人免疫球蛋白M (IgM)支架结合。
首席通讯作者Yi Shi博士及其同事概述了在小鼠身上进行的临床前试验,表明这些结构对致病性冠状病毒sarbecovirus(包括Omicron亚系)具有超强、广泛和持久的疗效,具有良好的临床前结果。
该团队与牛津大学和凯斯西储大学的研究人员合作,利用冷冻电子显微镜和冷冻断层扫描等先进的成像工具,揭示了AMETA结构通过几种意想不到的机制中和病毒,超出了通过与受体结合竞争而中和的经典机制。这些方法包括将病毒颗粒聚集在一起,结合到刺突蛋白的关键区域,并以其他抗病毒治疗方法未见的方式破坏刺突结构,以防止病毒感染细胞。通过低温电子显微镜和模型的结构分析揭示了单一结构中的多种抗病毒机制。在皮摩尔至纳摩尔浓度下,AMETA有效诱导与刺突蛋白和与病毒间交联,促进刺突蛋白融合后的病毒解除。这种多目标策略,加上结合强度的显著提高,为抵御不断进化的病毒提供了更持久、更有弹性的防御。AMETA的模块化使快速、经济高效的生产成为可能。
伊坎西奈山药理学副教授施说:“AMETA灵活的设计使其能够快速适应各种病原体,为新出现的感染提供灵活和动态的解决方案。”“我们的发现在克服病毒和耐抗生素微生物的突变逃逸方面迈出了重要一步。”“总的来说,这些结果强调了AMETA是一种模块化、有效和持久的策略,可以对抗具有挑战性的病原体。”
“我们的AMETA系统结合了IgM支架的强亲和性与Nbs的高特异性和卓越的生物工程潜力,Nbs的微小尺寸和小足迹使得AMETA结构能够与广泛的致病表位结合,包括小角落、缝隙和保守位点。”
“我们与AMETA的目标是创建一个持久的平台,克服病毒病原体快速发展的特性,”该研究的共同资深作者,Irene和Arthur M. Fishberg博士医学教授,伊坎西奈山全球健康和新兴病原体研究所所长Adolfo Garcia-Sastre博士指出。“这个平台不仅是COVID-19的解决方案,而且还可以作为一个框架,用于对抗其他快速变异的人类微生物,如艾滋病毒,并防止未来新出现的病毒,包括具有大流行潜力的流感病毒。AMETA灵活的设计使其能够快速适应各种病原体,为新出现的感染提供灵活和动态的解决方案。我们的发现在克服病毒和耐抗生素微生物的突变逃逸方面迈出了重要一步。”研究成果扩大了针对传染病和耐药系统的治疗策略的范围,为对抗各种病原体的创新方法铺平了道路。
由于AMETA的模块化结构,它还能够快速、经济地生产新的纳米体结构,使其成为解决未来流行病的理想候选药物。“AMETA的模块化能够实现快速、具有成本效益的生产,并适应不断进化的病原体。”Shi和Garcia-Sastre的团队现在正准备进行更多的临床前和潜在的临床试验,以评估AMETA对各种疾病的治疗潜力。
 生物通微信公众号
生物通微信公众号
生物通 版权所有