编辑推荐:
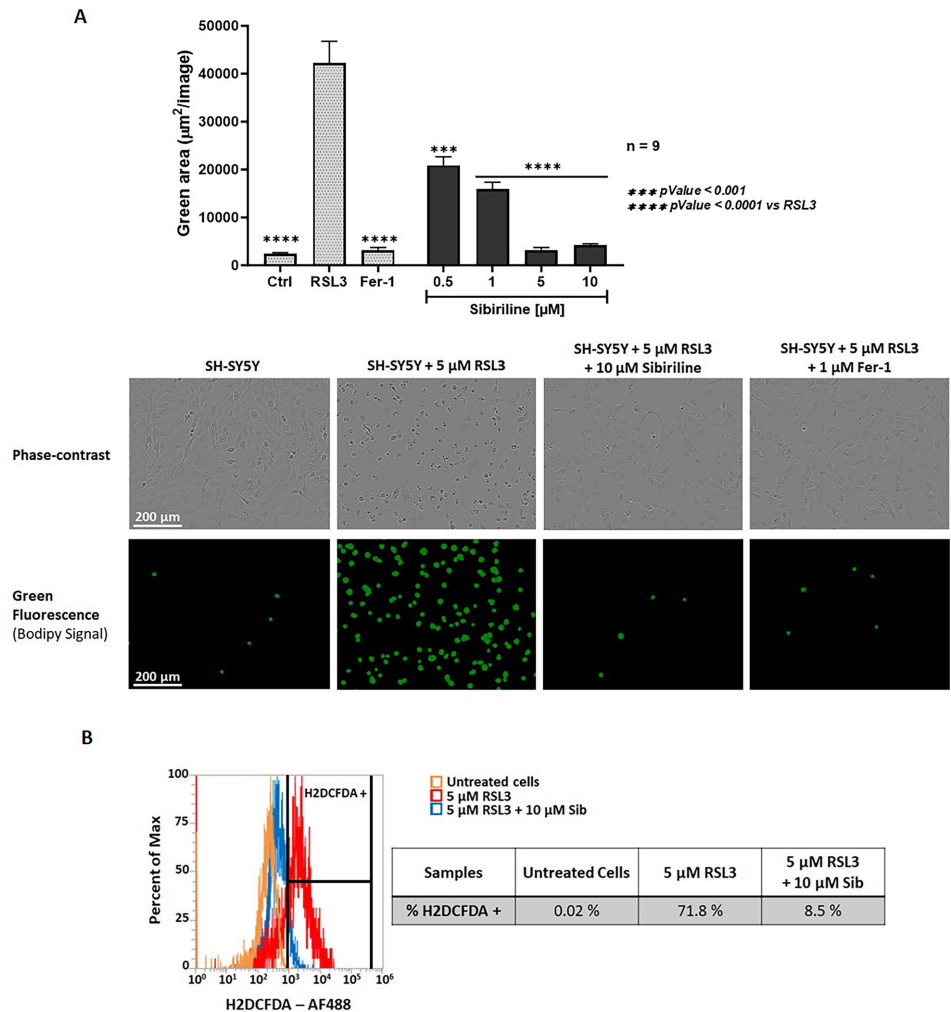
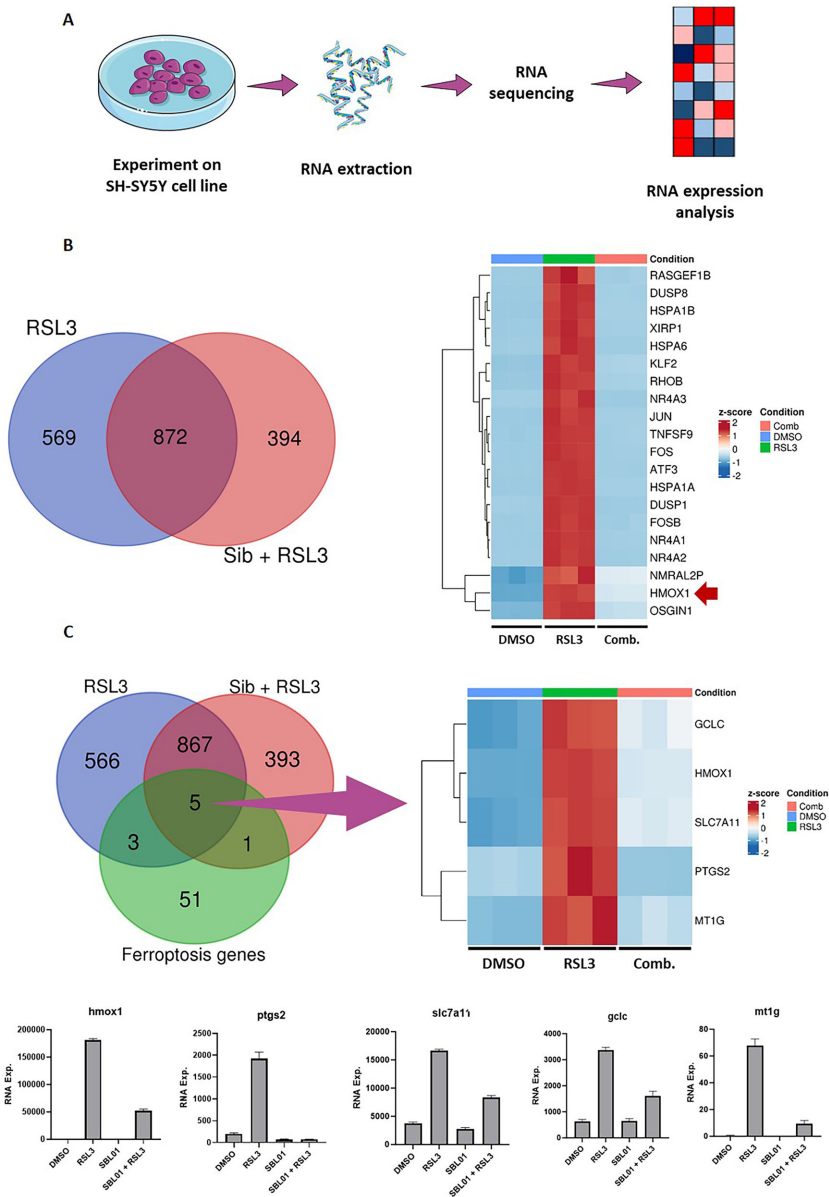
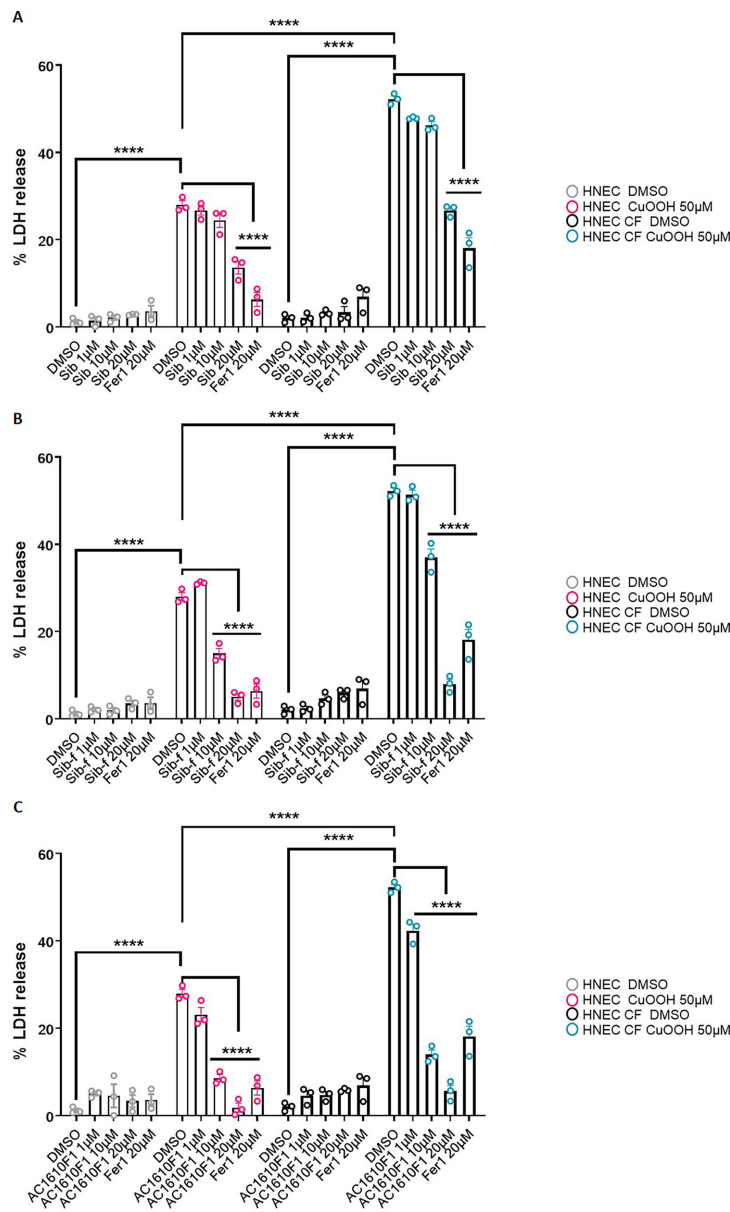
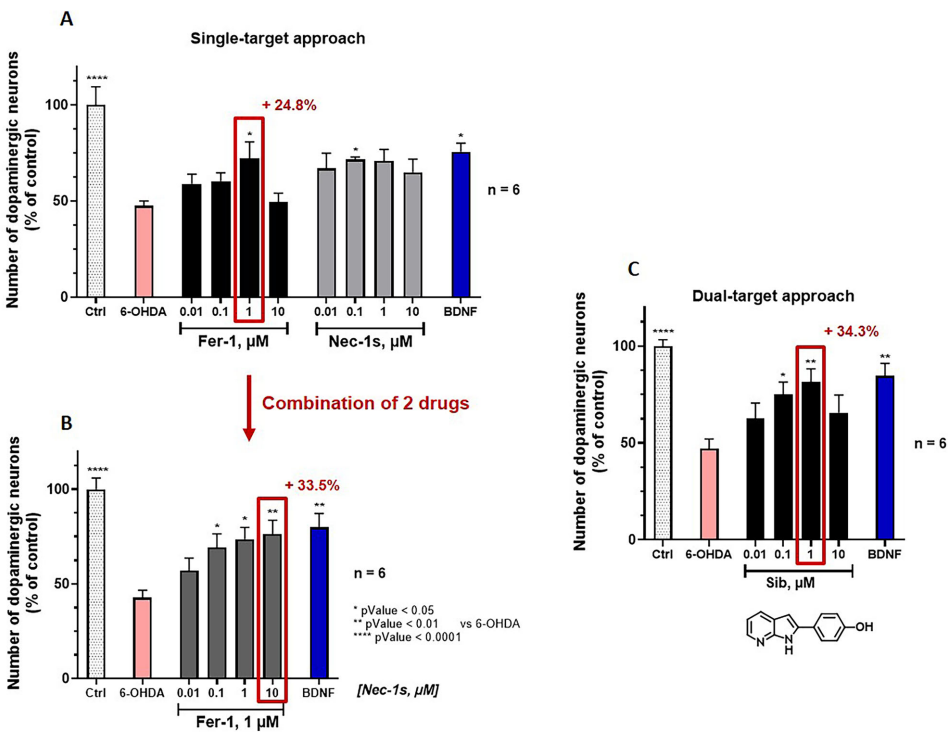
本期推荐一项关于程序性细胞死亡调控的创新研究。为解决坏死性凋亡(necroptosis)和铁死亡(ferroptosis)在多种严重急慢性疾病中协同激活且缺乏有效治疗手段的问题,研究人员聚焦于新型7-氮杂吲哚衍生物sibiriline(Sib)。研究发现Sib能通过双重机制发挥协同保护作用:抑制RIPK1激酶活性阻断坏死性凋亡通路,同时作为自由基捕获抗氧化剂(RTA)直接抑制磷脂过氧化(pLPO)从而阻断铁死亡。在帕金森病和囊性纤维化疾病模型中,Sib展现出显著的治疗潜力,为开发"RIPROStains"类多靶点药物提供了新策略。
生物通 版权所有