编辑推荐:
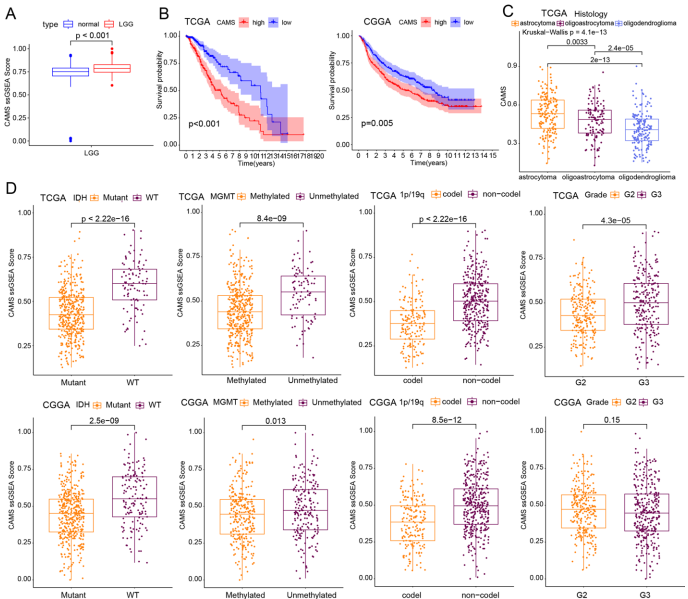
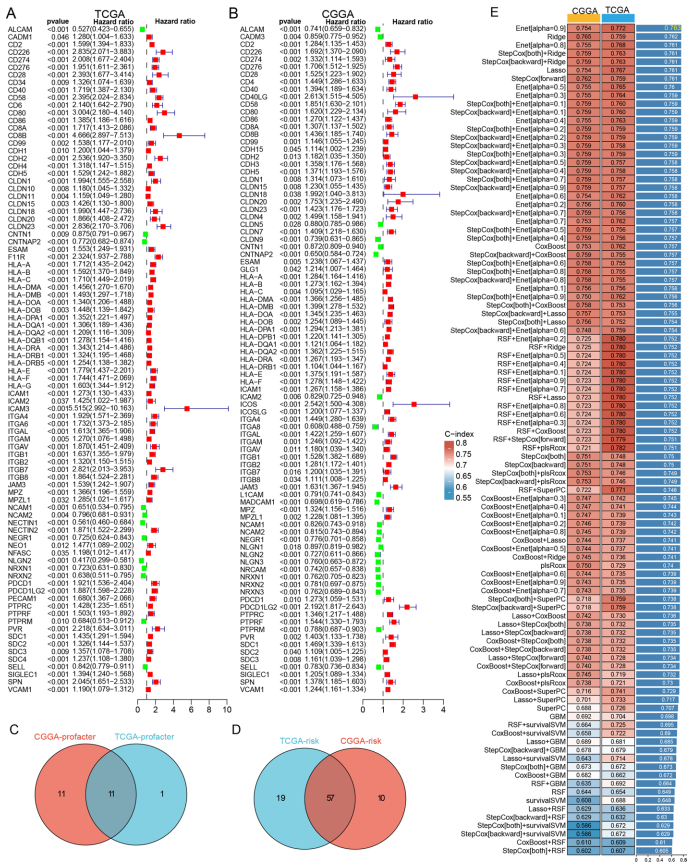
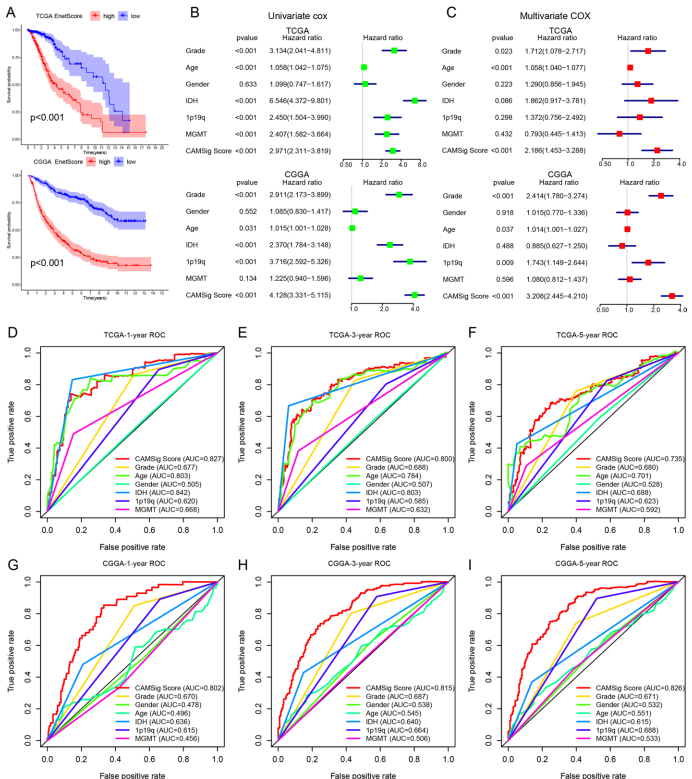
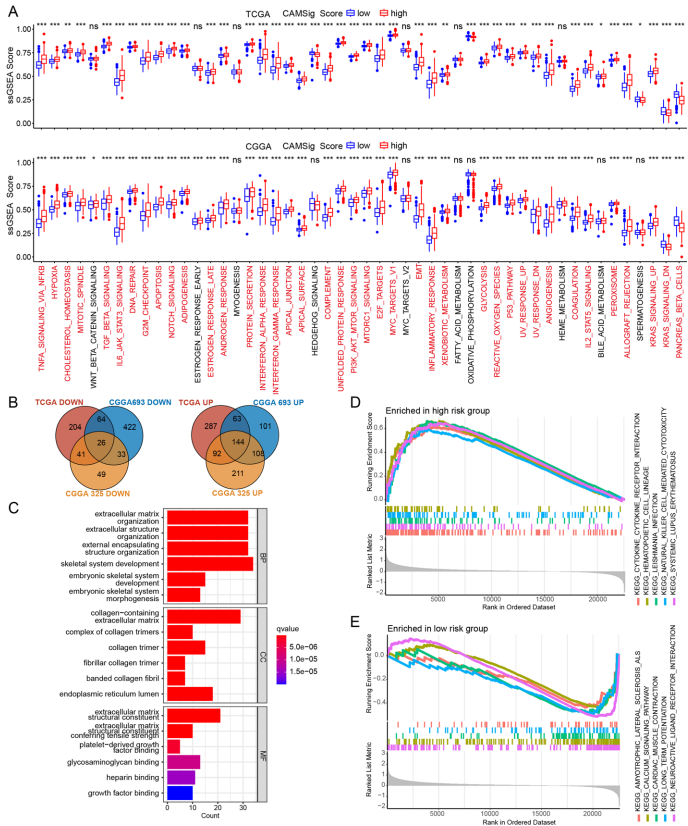
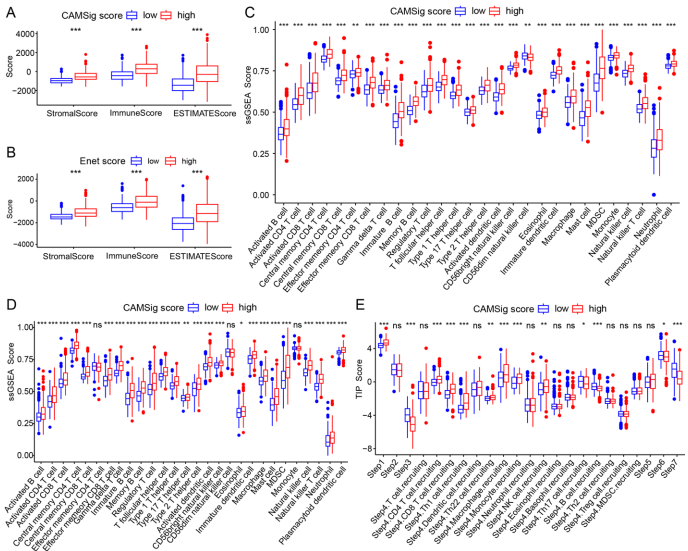
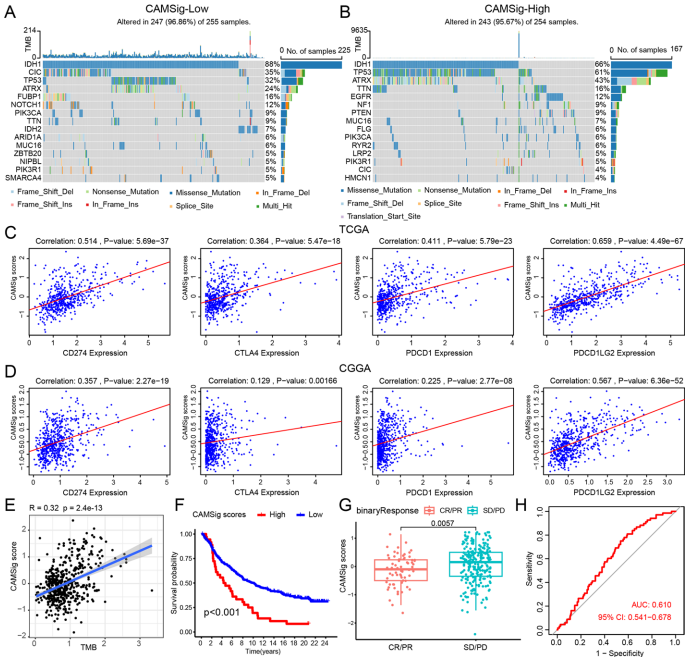
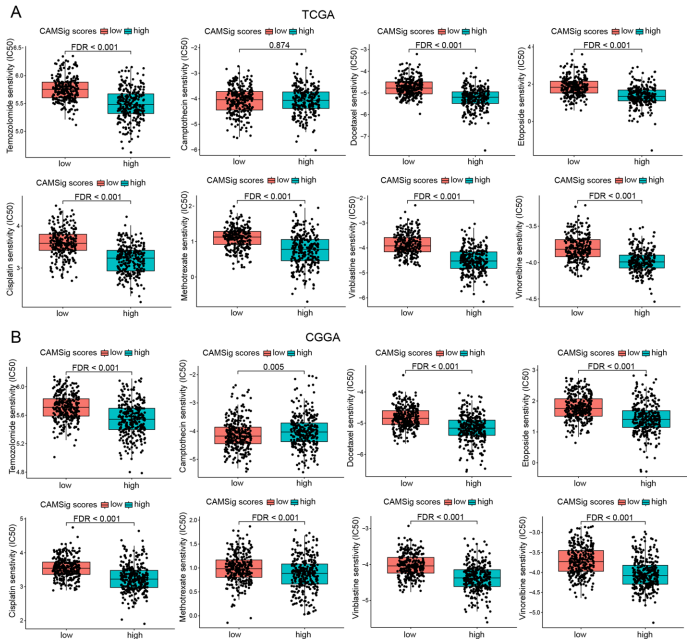
本研究针对细胞黏附分子(CAMs)在低级别胶质瘤(LGGs)预后评估和临床潜力尚未充分探索的问题,通过整合TCGA和CGGA多组学数据,结合10种机器学习算法构建了包含13个关键基因(如CD58、ITGB1、VCAM1)的CAM相关预后标志(CAMSig)。研究发现CAMSig能有效区分患者风险群体,其预测准确性优于IDH突变、1p/19q共缺失等传统生物标志物,并揭示高风险组患者表现出上皮间质转化(EMT)、PI3K-AKT信号通路激活及免疫抑制微环境特征。重要的是,CAMSig可预测免疫检查点阻断(ICB)疗法耐药性和替莫唑胺(TMZ)化疗敏感性,为LGG精准治疗提供新策略。
生物通 版权所有