编辑推荐:
这篇综述深入探讨了潘氏细胞(PCs)在肠道微生物群稳态中的关键作用及其与心血管疾病(CVD)的关联机制。文章系统阐述了PCs通过分泌抗菌肽(AMPs)调控肠道屏障功能,而PCs功能障碍会导致微生物群失调,促进三甲胺N-氧化物(TMAO)等促炎代谢物产生,最终通过"肠-心轴"加剧动脉粥样硬化、高血压和心力衰竭等CVD。综述还总结了靶向PCs功能(如溶菌酶补充、SCFAs调节)和TMAO抑制剂等新型治疗策略,为CVD防治提供了新视角。
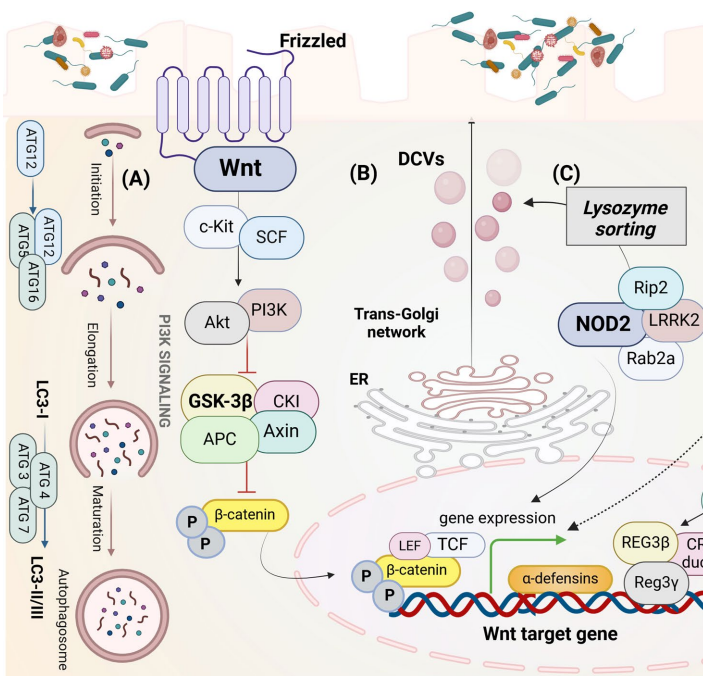
潘氏细胞(PCs)作为小肠隐窝底部的特殊分泌细胞,通过分泌溶菌酶、α-防御素等抗菌肽(AMPs)构成肠道第一道防线。这些AMPs能选择性抑制病原体生长,同时维持共生菌群平衡。值得注意的是,PCs通过NOD2/TLRs信号通路感知肠道微生物,其中NOD2识别细菌肽聚糖成分MDP后,通过NF-κB通路调控AMPs表达。TLR-9则通过TRIF-MyD88适配蛋白上调防御素基因表达。
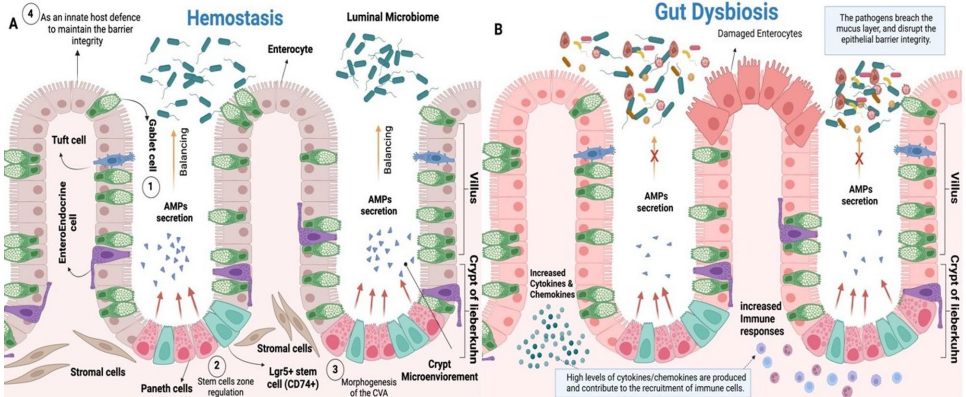
当PCs功能受损时,肠道菌群失衡导致两种关键代谢物变化:促动脉粥样硬化的TMAO水平升高,而具有心脏保护作用的短链脂肪酸(SCFAs)减少。动物实验显示,补充胆碱(1.2%)或TMAO(0.12%)的饮食会显著加重心衰症状。临床研究发现,高血压患者接受粪菌移植(FMT)后,收缩压平均降低4.34mmHg,尤其对48岁以上患者效果显著。
针对PCs功能障碍的干预措施包括:
多项临床研究证实PCs相关生物标志物与CVD的关联:
最新研究发现PCs能分泌VEGF-A/C/D等促血管生成因子,在门静脉高压模型中调控肠系膜血管密度。通过他莫昔芬诱导PCs完全缺失后,门静脉压力显著降低,这揭示了PCs在血管重塑中的非经典功能。
当前证据表明PCs通过三条核心通路影响CVD:
生物通 版权所有