编辑推荐:
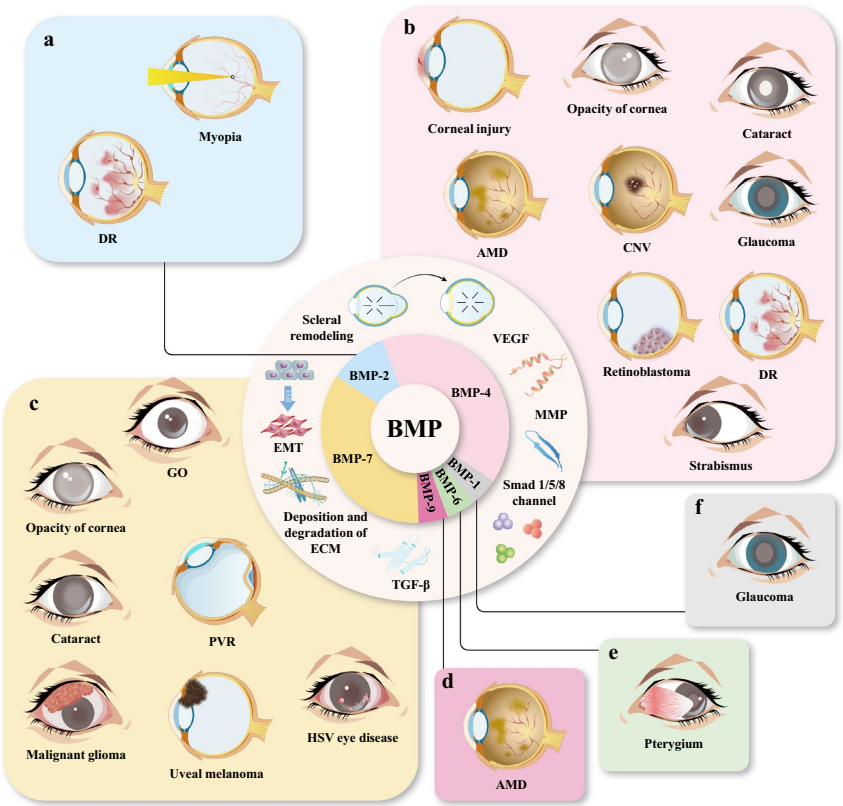
这篇综述系统阐述了骨形态发生蛋白(BMPs)在眼部发育和疾病治疗中的双重作用。作为TGF-β超家族成员,BMPs通过经典Smad通路调控角膜纤维化、青光眼、年龄相关性黄斑变性(AMD)等疾病的进程,其拮抗TGF-β的特性为抗纤维化和抑制上皮-间质转化(EMT)提供了新策略。文章整合20年动物模型和体外实验证据,揭示了BMP-2/4/7等亚型在近视、斜视、白内障等疾病中的治疗潜力,同时指出载体递送和剂量优化等临床转化挑战。
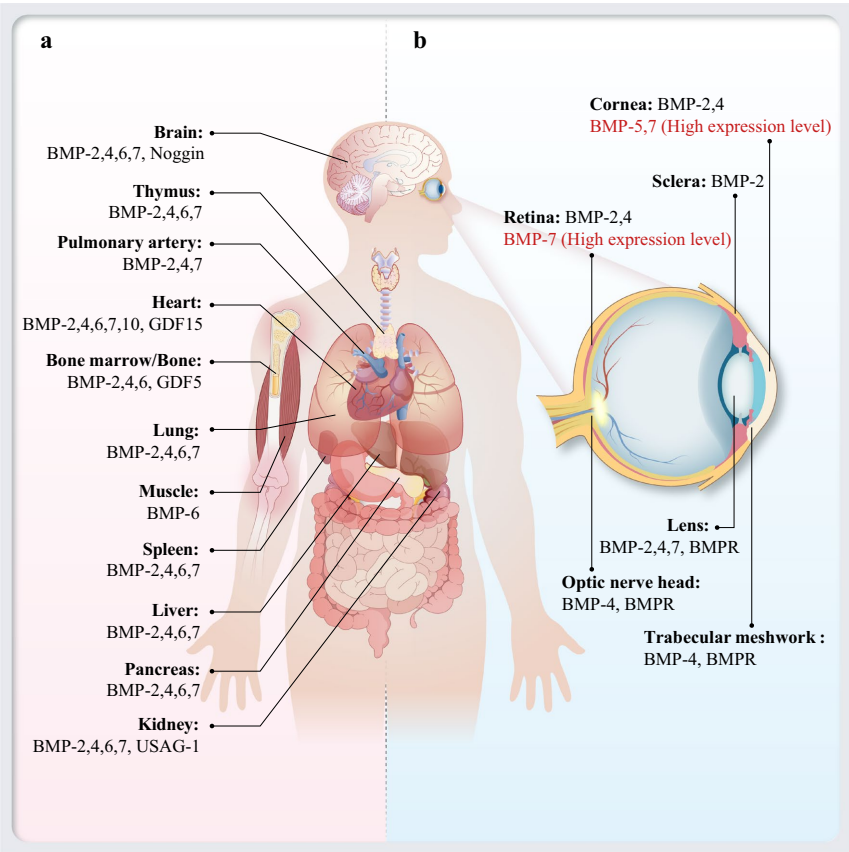
骨形态发生蛋白(BMPs)作为TGF-β超家族的重要成员,最初因诱导骨和软骨形成的能力被发现。随后的研究揭示,BMPs在胚胎发育和成人组织稳态中发挥核心作用,其表达谱覆盖角膜、视网膜、晶状体等眼部组织。BMP-2、4、5、7等亚型通过BMPR-IA/IB和BMPR-II受体激活Smad1/5/8信号通路,参与调控细胞增殖、分化和ECM重塑。这种广泛的分布暗示BMPs可能成为眼部疾病治疗的靶点。
近视全球患者预计2050年达48亿,其病理核心是巩膜重塑导致的眼轴延长。研究发现,豚鼠近视模型中BMP-2/5表达下调,通过HSFs实验证实BMP-2可促进I/III型胶原合成,同时抑制MMP-2活性,增强巩膜刚度。值得注意的是,BMP-2与脉络膜厚度呈负相关,ID3基因作为其下游标志物,可能成为近视进展的生物标记。
在兔眼外肌注射BMP-4可产生持续肌力减弱效应。临床研究显示,间歇性外斜视患者内直肌中BMP-4与MMP-2/9水平正相关,而TIMP表达负相关,提示BMP-4可能通过调节ECM平衡影响手术预后。
角膜损伤后,BMP-7通过激活Smad1/5/8拮抗TGF-β诱导的EMT,抑制α-SMA和纤维连接蛋白表达。金纳米颗粒(PEI2-GNP)递送BMP-7基因可减少碱烧伤模型的角膜混浊,其机制与上调Smad6有关。BMP-4则通过抑制NETs形成和顶端连接复合体损伤,阻断角膜新生血管(CoNV),且相比抗VEGF药物更利于上皮修复。
研究呈现矛盾结论:BMP-7过表达限制肿瘤侵袭范围,而BMP-2/4通过Smad1/5激活促进黑色素瘤EMT。这种亚型特异性效应可能与肿瘤微环境相关,提示需精确调控BMP亚型选择。
生物信息学筛选发现BMP1可能是潜在标志物。在TM细胞中,BMP-4与TGF-β2形成动态平衡——BMP-4抑制ECM沉积,而其拮抗剂gremlin则增强TGF-β2效应,该自分泌环路异常可能导致房水流出阻力增加。
BMP-7剂量依赖性地阻断TGF-β2诱导的晶状体上皮EMT。Notch通路被证实是BMP-4/7抑制细胞迁移的关键机制,为白内障药物开发提供新方向。
尽管BMPs展现出多重治疗潜力,其临床应用仍面临三大瓶颈:天然BMPs提取成本高且易降解;重组蛋白治疗窗窄,可能引发炎症;现有载体系统如胶原、纳米颗粒尚未完美解决靶向递送问题。未来研究需聚焦亚型特异性机制、优化给药方案,并推动转化医学验证。
生物通 版权所有