编辑推荐:
本研究为解决离子液体(ILs)在生物医学应用中缺乏系统性生物安全性评估的问题,研究人员通过构建模块化ILs库,揭示了阳离子烷基链长度(C)对细胞毒性的主导作用,首次证实ILs在水环境中形成纳米聚集体(scILs/lcILs)的生物学行为差异,阐明了lcILs通过靶向线粒体诱导线粒体自噬(mitophagy)和凋亡(apoptosis)的分子机制,为ILs的精准生物医学应用提供了理论依据。
在追求绿色化学与可持续材料的浪潮中,离子液体(ILs)因其可设计的结构和独特的物理化学性质备受关注。然而,这种"万能溶剂"在生物医学领域的应用却长期面临瓶颈——缺乏系统性生物安全性评估标准,特别是其纳米尺度行为与生物体系的相互作用机制仍是未解之谜。当科学家们试图将ILs应用于药物递送或肿瘤治疗时,往往陷入"盲人摸象"的困境:某些ILs表现出优异的生物相容性,而另一些却引发严重毒性,这种差异背后的结构-活性关系始终未能阐明。
中国科学院过程工程研究所(Institute of Process Engineering, Chinese Academy of Sciences)的研究团队在《Nature Communications》发表的研究,通过构建包含61种ILs的模块化库,首次揭示了阳离子烷基链长度(C)是决定ILs生物相容性的关键因素。研究发现短链ILs(scILs)和长链ILs(lcILs)在水溶液中均会形成纳米聚集体,但两者在细胞内的命运截然不同:scILs被限制在囊泡内保持惰性,而lcILs能突破膜屏障靶向线粒体,通过破坏线粒体膜电位诱发线粒体自噬和凋亡。这种"纳米尺度分道扬镳"的现象,在从细胞系、类器官到小鼠、犬类等多层次实验模型中均得到验证。
研究团队运用了多项关键技术:通过冷冻透射电镜(Cryo-TEM)首次捕获ILs纳米聚集体的原始形态;结合分子动力学(MD)模拟阐明lcILs穿透线粒体双膜屏障的分子机制;利用患者来源肝癌类器官(PDOs)和三维肿瘤球模型评估临床相关性;通过STED超分辨显微镜实时追踪纳米聚集体亚细胞定位;建立机器学习模型预测ILs结构-毒性关系。
阳离子烷基链长度主导ILs毒性效应
通过系统筛选61种模块化设计的ILs(变异组合包括阳离子侧链C、阳离子头H和阴离子A),发现所有测试细胞系(bEnd.3、4T1、HepG2)的存活率均随阳离子烷基链碳原子数增加而降低。机器学习模型预测显示,C1-C4 ILs几乎无细胞毒性,而碳链≥8的ILs毒性显著升高。这一规律在三维HepG2肿瘤球和患者来源肝癌类器官中得到验证——C12MIMCl处理组细胞存活率<5%,而C3MIMCl组保持100%活性。
ILs纳米聚集体的实验证实与细胞互作
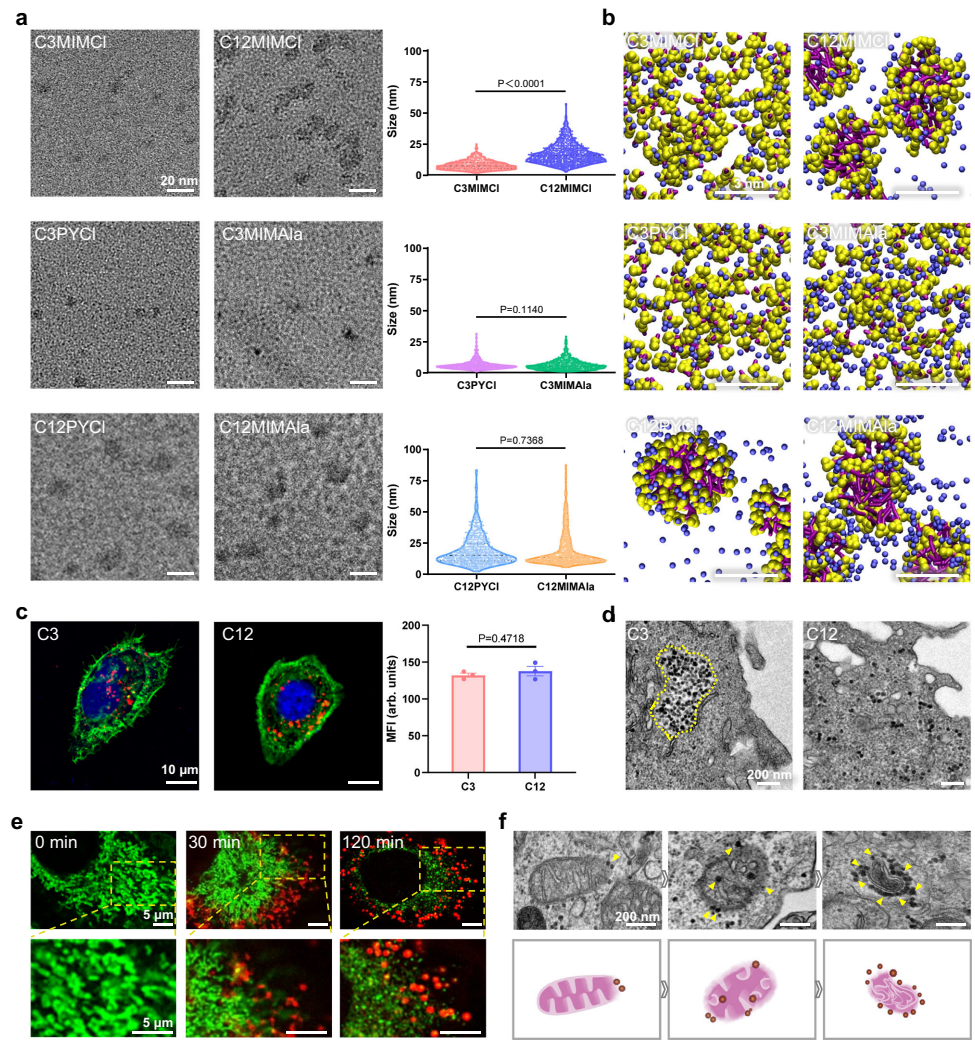
线粒体靶向引发的级联毒性机制
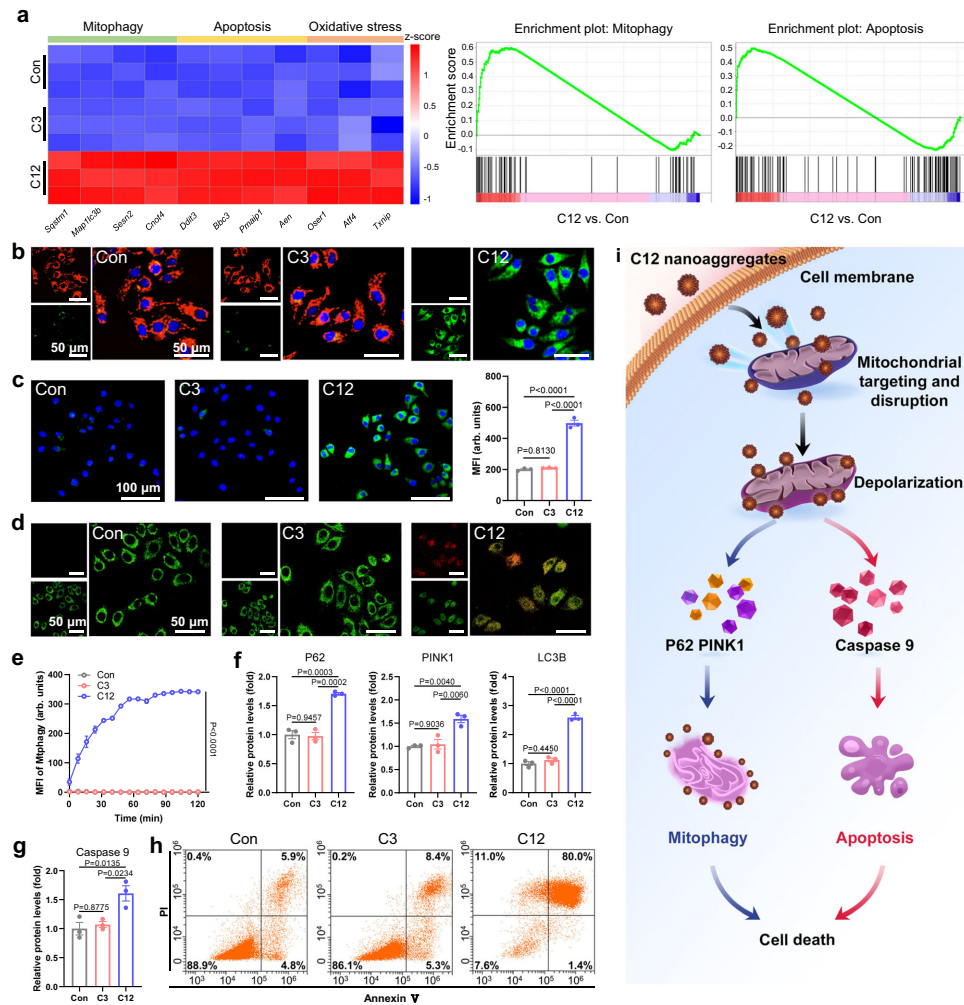
纳米聚集体穿透线粒体膜的分子机制

多物种验证的毒性差异与转化应用
小鼠实验显示scILs的耐受剂量显著高于lcILs(口服80倍,肌注67倍,静脉25倍)。犬类模型证实C12MIMCl引发呕吐、腹泻等急性胃肠毒性,而C3MIMCl表现安全。利用scILs纳米聚集体负载难溶性药物醋酸甲地孕酮,其口服生物利用度较商业片剂提高3.1倍,突破性解决了该抗癌药长期存在的吸收难题。
这项研究建立了ILs结构-活性的定量关系,填补了纳米聚集体生物效应机制的知识空白。其意义不仅在于为ILs的生物医学应用划定安全边界,更开创性地提出了"纳米聚集体生物学"的新概念——离子液体的生物效应必须从其纳米组装形态而非单一分子层面理解。该成果为设计新一代智能离子液体药物递送系统提供了理论框架,同时警示长链ILs的环境风险需严格管控。中国科学院过程工程研究所开发的模块化ILs库与多尺度评价体系,将成为未来ILs生物安全性研究的黄金标准。
生物通 版权所有