编辑推荐:
这篇综述系统梳理了AHDC1基因的结构、功能及其在Xia-Gibbs综合征(XIGIS)中的作用,揭示了该基因在神经发育、染色质调控和代谢中的多效性。通过整合进化分析、表达谱和突变数据,作者提出AHDC1可能通过液-液相分离(LLPS)参与基因表达调控,为理解其分子机制和开发精准治疗策略提供了新视角。
AHDC1基因的发现可追溯至2014年,当时Richard A. Gibbs团队在Baylor医学院首次将其与罕见神经发育障碍Xia-Gibbs综合征(XIGIS)相关联。尽管人类基因组计划完成已逾二十年,AHDC1仍属于长期被忽视的"暗基因"(Tdark gene),直到2023年才因研究突破被重新归类为"生物候选基因"(Tbio gene)。这种编码1603个氨基酸的核蛋白,通过其独特的AT-hook DNA结合基序和PDZ结构域,在染色质组织和基因调控中扮演关键角色。
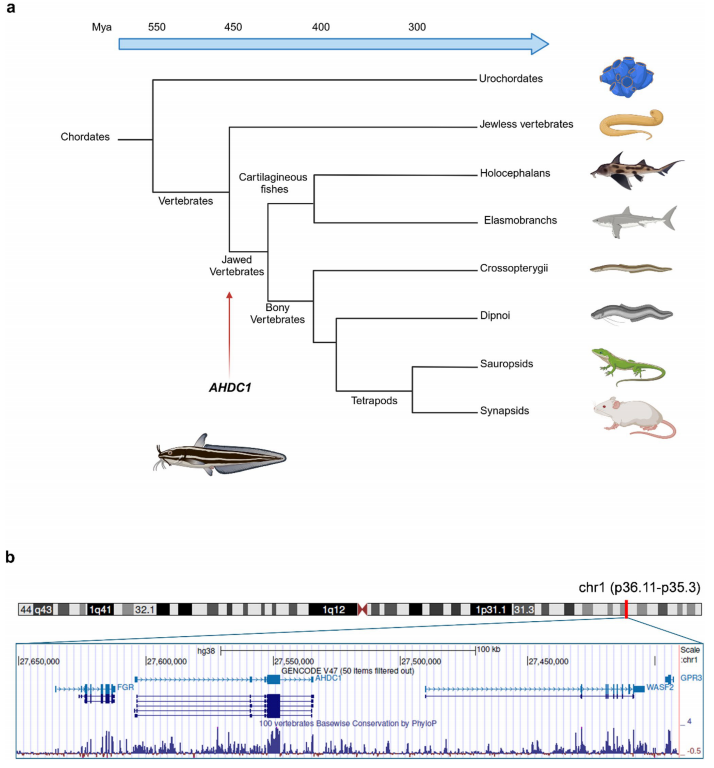
进化分析显示,AHDC1最早出现在4.5亿年前的软骨鱼类中,与有颌脊椎动物髓鞘形成的关键进化事件同步。该基因在1p36.11-p35.3染色体区域保持高度保守的基因连锁群,两侧始终为FGR和WASF2基因。其独特的单外显子编码结构在100多种脊椎动物中完全保留,提示该区域可能存在重要的调控元件。转录本分析揭示,AHDC1通过可变5'非翻译外显子和高度保守的3'UTR实现复杂调控,ENCODE数据证实其启动子区域在人类胚胎干细胞中具有DNase I超敏感位点。
GTEx和BrainSpan数据库显示,AHDC1在全组织广泛表达,但在小脑中表达量最高。发育时序分析发现,其表达在胚胎21周达到峰值,恰逢小脑颗粒细胞大量产生的关键期。值得注意的是,视黄酸(RA)可诱导AHDC1表达,这种形态发生素正是小脑神经元分化的核心调控因子。小鼠模型证实Ahdc1在E11.5和E16.5胚胎脑中活跃表达,进一步支持其在神经发育中的保守功能。
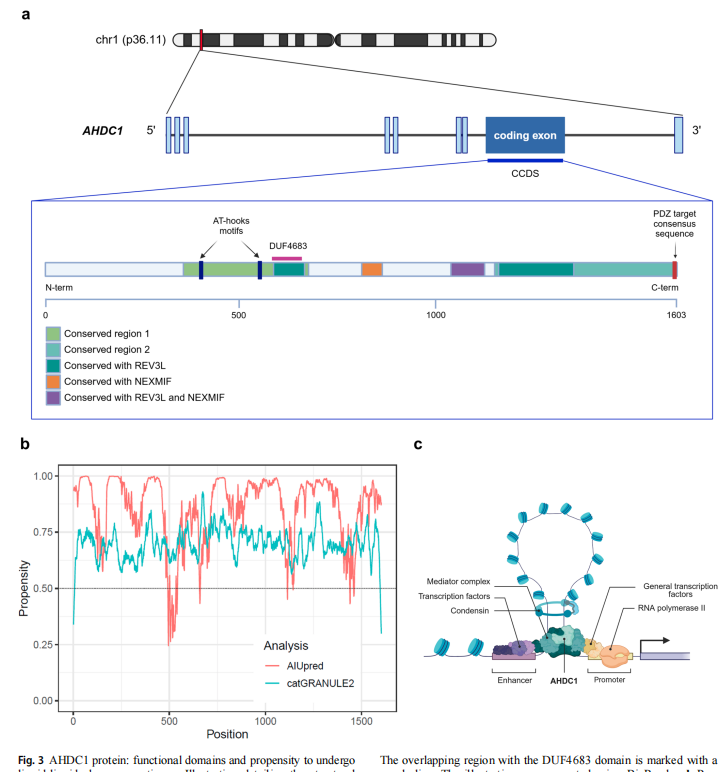
AHDC1蛋白含有两个AT-hook结构域(396-408, 544-556)和一个C端PDZ结合域。计算预测显示70%以上的序列为内在无序区域(IDRs),catGRANULE2算法强烈提示其具有液-液相分离(LLPS)能力。实验证据表明,AHDC1通过维持增强子-启动子染色质互作调控上皮形态发生,缺失会导致CTCF结合减少和DNA甲基化异常。在尤文肉瘤中,AHDC1与BRD4/BRG1共定位,可能稳定致癌转录因子复合物。
目前已报道97例XIGIS患者携带AHDC1突变,包括无义突变(如p.Arg151)、移码突变(如p.Ser215Lysfs16)和错义突变(如p.Arg487Trp)。值得注意的是,C端突变通常与严重表型相关,而位于第二AT-hook结构域(p.Gly537Asp)和REV3L同源区(p.Asp607Asn)的错义突变则与癫痫高发相关。5'UTR突变(c.-781C>G)会升高基因表达,导致阻塞性睡眠呼吸暂停等特殊症状。
AHDC1与自闭症(ASD)和精神分裂症(SZ)存在双重关联:SFARI数据库将其列为1S级ASD风险基因,而两项独立研究报道了AHDC1突变与散发性SZ的关联。动物模型显示,Ahdc1+/-小鼠出现肥胖和胰岛素抵抗,而纯合缺失导致胚胎致死。基于突变类型差异,精准治疗策略需个性化设计:对功能获得性突变可采用等位特异性siRNA沉默,而对单倍剂量不足病例则可尝试SINEUP RNA提升翻译效率。
AHDC1代表了一类多功能调控因子,其通过染色质重塑、相分离和代谢调控参与多种生理病理过程。未来研究需着重解析其相分离的分子机制,开发靶向干预策略,并探索其在髓鞘形成中的潜在作用——这一功能可能从4.5亿年前基因起源时就已奠定。
生物通 版权所有