编辑推荐:
这篇综述深入探讨了APOE基因型(特别是APOE4)通过调控脑能量代谢(如糖酵解、线粒体功能和胰岛素信号通路)影响阿尔茨海默病(AD)病理进程的机制。文章系统分析了APOE异构体(E2/E3/E4)对神经元和星形胶质细胞代谢的差异化调控,提出APOE4可能通过早期高代谢向晚期低代谢的转换加速AD发展,为靶向代谢干预提供了新视角。
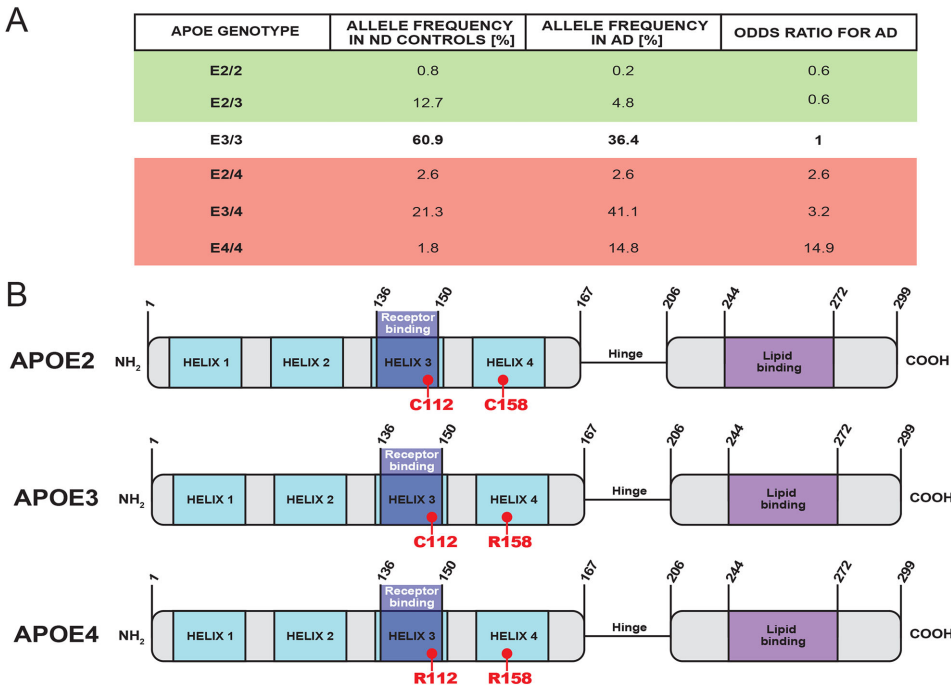
人类大脑作为高耗能器官,占体重2%却消耗全身20%能量。阿尔茨海默病(AD)作为最常见的神经退行性疾病,其病理特征包括β-淀粉样蛋白(Aβ)沉积和神经纤维缠结。APOE基因的ε4等位基因(APOE4)是散发性AD最强的遗传风险因子,而APOE2则具有保护作用。APOE不仅是脑内主要脂质载体,还参与免疫反应、突触可塑性和能量代谢调控。
神经影像学研究显示,AD患者大脑特定区域(如颞顶叶皮层)存在显著的葡萄糖低代谢,且与淀粉样蛋白沉积呈负相关。FDG-PET技术证实,这种代谢异常甚至早于临床症状出现20-30年。值得注意的是,APOE4携带者表现出更快的Aβ沉积速率和更高的tau蛋白负荷,提示代谢紊乱与病理进程密切相关。
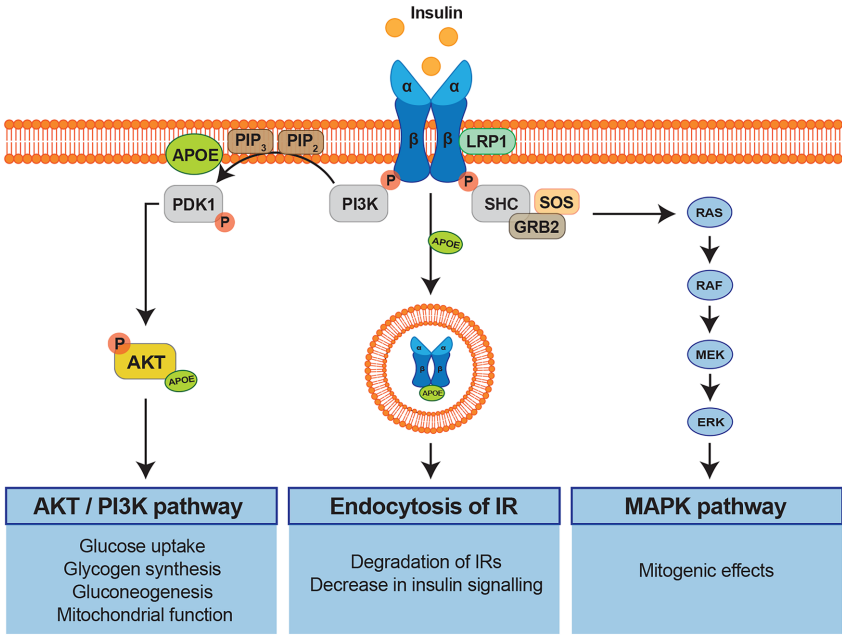
APOE4通过多重机制干扰胰岛素信号:
与胰岛素受体(IR)竞争性结合,抑制IR内化和AKT磷酸化
促进IRS-1在S636/639位点的磷酸化
通过LRP1下调细胞表面GLUT4表达
研究显示,APOE4-IR相互作用随年龄增强,导致老年APOE4携带者脑胰岛素抵抗加剧。
在神经元中,APOE4引起:
己糖激酶(HK1/HK2)表达和活性降低
磷酸果糖激酶(PFK)和丙酮酸激酶(PKM1)代偿性上调
乳酸生成减少(N2a-APOE4细胞较APOE2低30%)
星形胶质细胞则表现为:
葡萄糖摄取障碍但糖酵解通量增加
戊糖磷酸途径(PPP)活性增强
乳酸脱氢酶(LDH)活性升高
APOE4通过以下方式损害线粒体:
降低呼吸链复合体(特别是复合体IV)表达
增加DRP1介导的线粒体分裂
诱导线粒体-内质网连接(MAM)过度活化
在APOE4转基因小鼠中,线粒体代谢产物(苹果酸、柠檬酸)异常积累,伴随ATP合成代偿性增加,这种"高代谢状态"可能加速神经元耗竭。
最新证据支持APOE4诱导的双相代谢模式:青年期表现为:
葡萄糖摄取增加
糖酵解通量提升
线粒体呼吸增强
随着病理进展,逐渐转为:
GLUTs表达下调
OXPHOS能力下降
代偿性脂肪酸β氧化增强
这种转换可能解释临床观察到的早期高代谢与晚期低代谢矛盾现象。

靶向APOE4特异性代谢缺陷的策略包括:
PGC-1α激活剂改善线粒体生物合成
小分子抑制剂阻断APOE4结构域相互作用
酮体补充疗法(但对APOE4携带者效果有限)
值得注意的是,APOE2表现出独特的神经保护作用,其增强糖酵解和酮体利用的能力可能成为治疗开发的蓝本。
关键问题仍需探索:
APOE2对胰岛素信号的正向调控机制
代谢转换的具体分子开关
星形胶质细胞-神经元代谢偶联的时空特异性
解决这些问题将推动AD精准治疗的发展。
生物通 版权所有