编辑推荐:
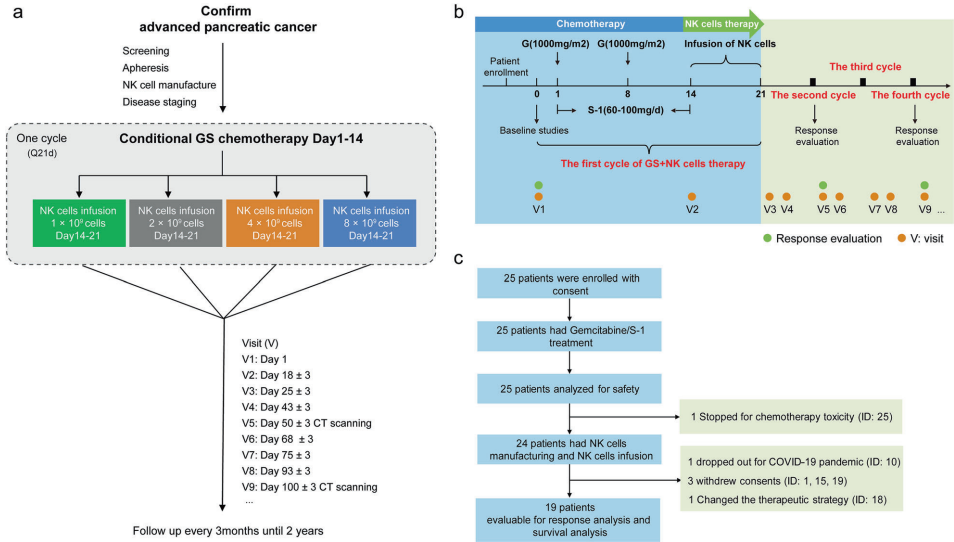
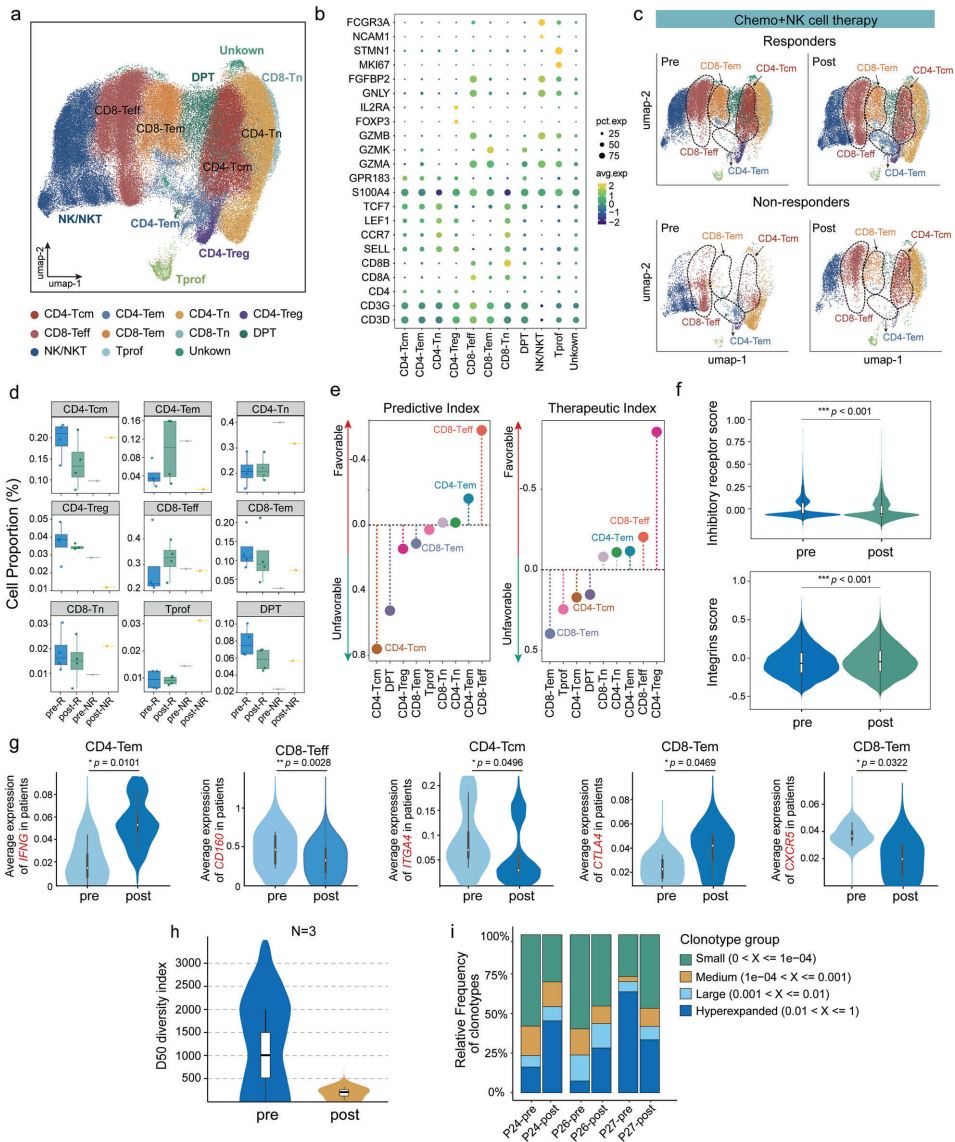
【编辑推荐】为突破晚期胰腺癌(APC)免疫治疗瓶颈,本研究开展了一项首次人体Ib/II期临床试验,探索异体NK细胞联合吉西他滨+S-1(GS)方案的安全性与疗效。研究证实该联合方案安全性良好(无GVHD/DLT),客观缓解率(ORR)达31.6%,且通过纵向单细胞RNA测序(scRNA-seq)发现响应者外周血中活化NK细胞亚群(c4-ZEB2、c6-IL15等)及效应T细胞(CD8+ Teff、CD4+ Tem)扩增,伴随T细胞克隆扩张。该研究为NK细胞疗法在实体瘤中的免疫调控机制提供了高分辨率动态图谱。
生物通 版权所有