编辑推荐:
本综述系统解析糖基化、磷酸化等PTMs如何调控PD-1/PD-L1等免疫检查点的稳定性与功能(如PD-1 N58糖基化),揭示这些修饰通过影响免疫检查点抑制剂(ICIs)疗效导致肿瘤免疫逃逸的机制,并创新性提出靶向UFMylation、乳酸化等新兴PTMs的治疗策略,为克服免疫治疗耐药提供新视角。
免疫检查点抑制剂(ICIs)如抗CTLA-4和抗PD-1/PD-L1抗体已变革癌症治疗,但低应答率和耐药性仍是挑战。蛋白翻译后修饰(PTMs)通过调控免疫检查点的表达、定位和功能,显著影响免疫治疗效果。本文综述了PTMs对免疫检查点的调控机制及靶向策略。
负向免疫调节分子
正向免疫调节分子
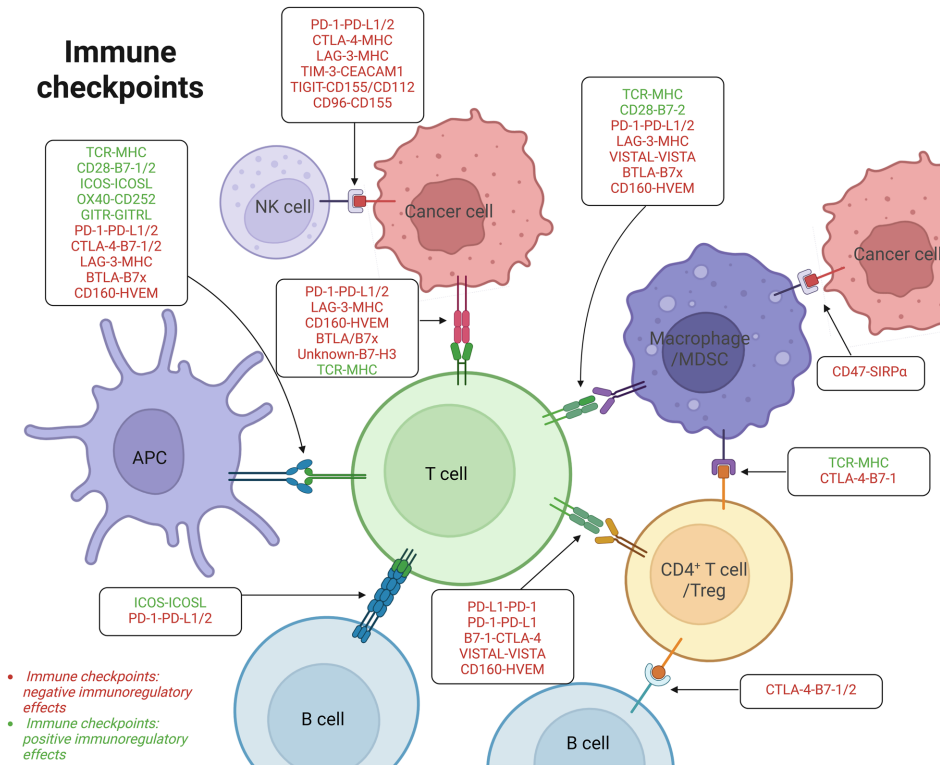
经典PTMs
糖基化(Glycosylation)
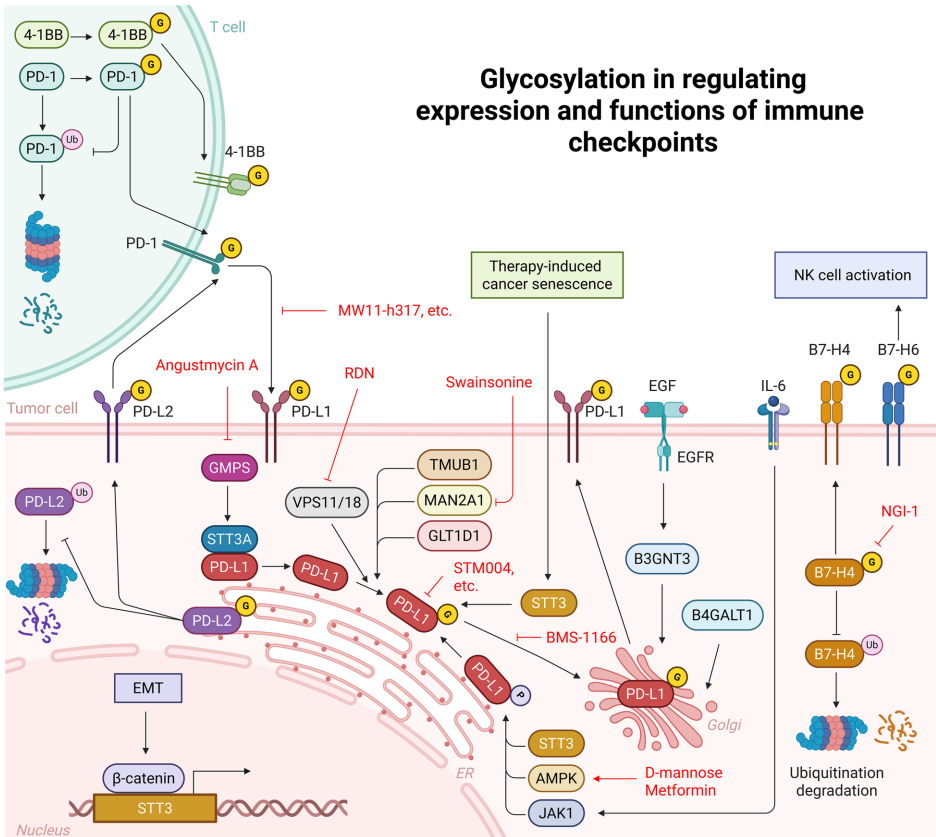
磷酸化(Phosphorylation)
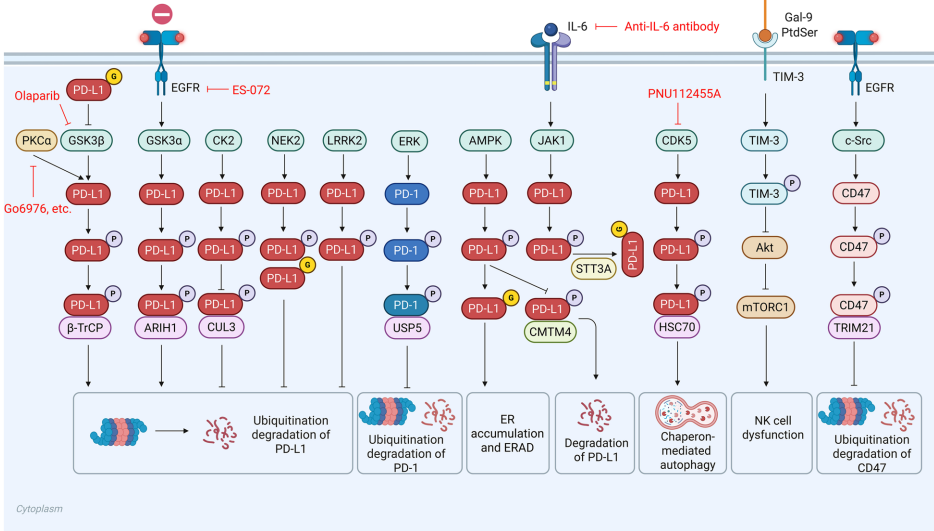
泛素化(Ubiquitination)
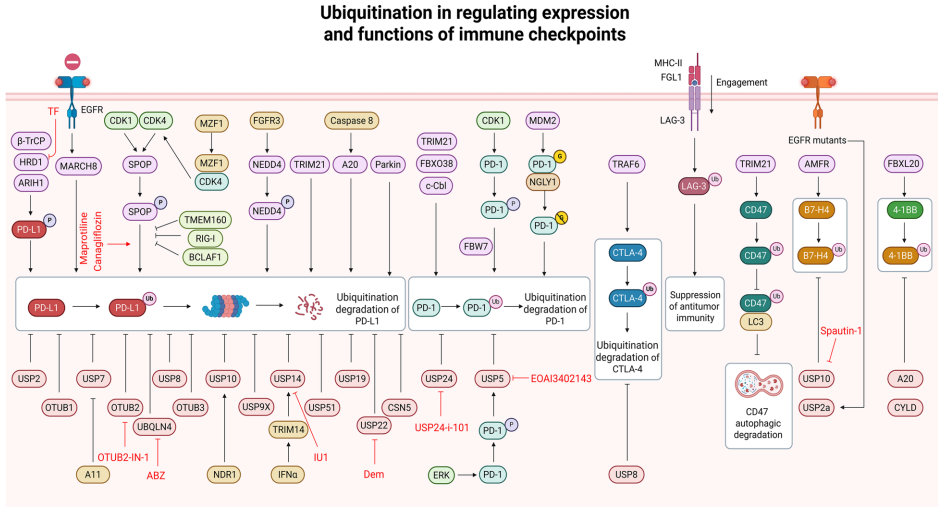
新兴PTMs
酰化修饰
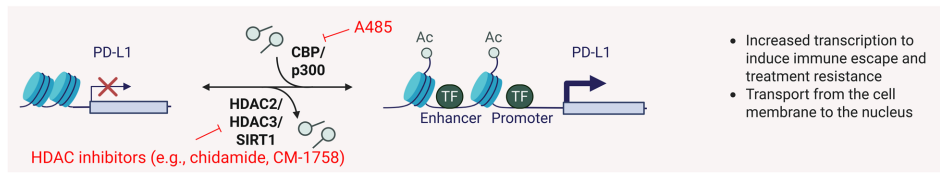
代谢相关修饰
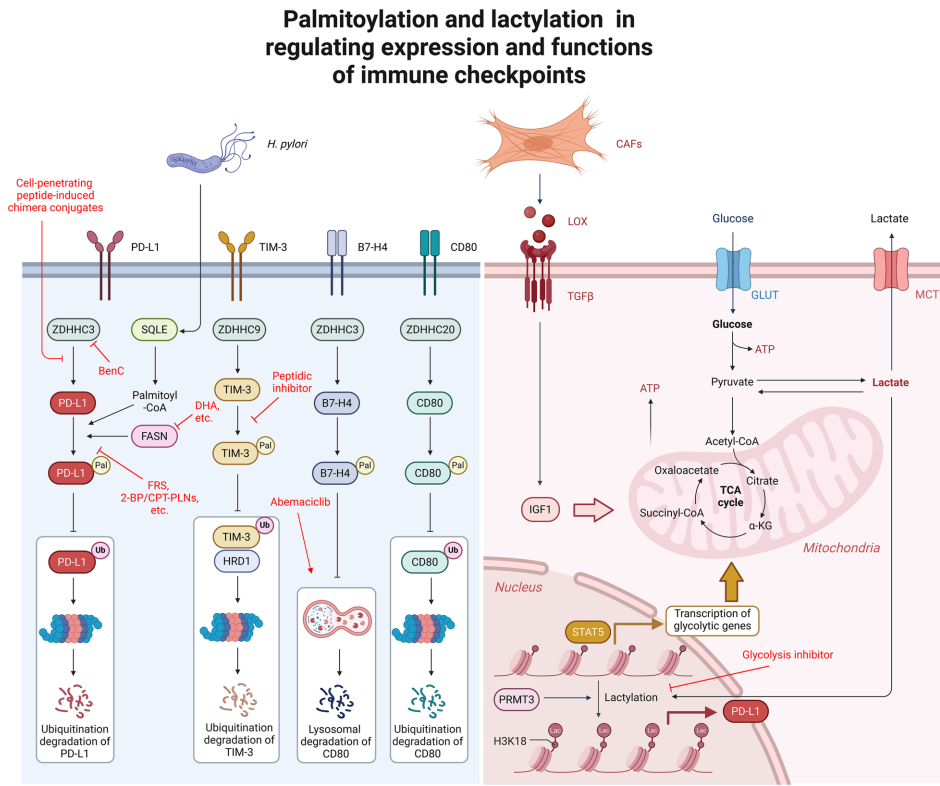
棕榈酰化(Palmitoylation)
泛素样修饰
 生物通微信公众号
生物通微信公众号
生物通 版权所有