编辑推荐:
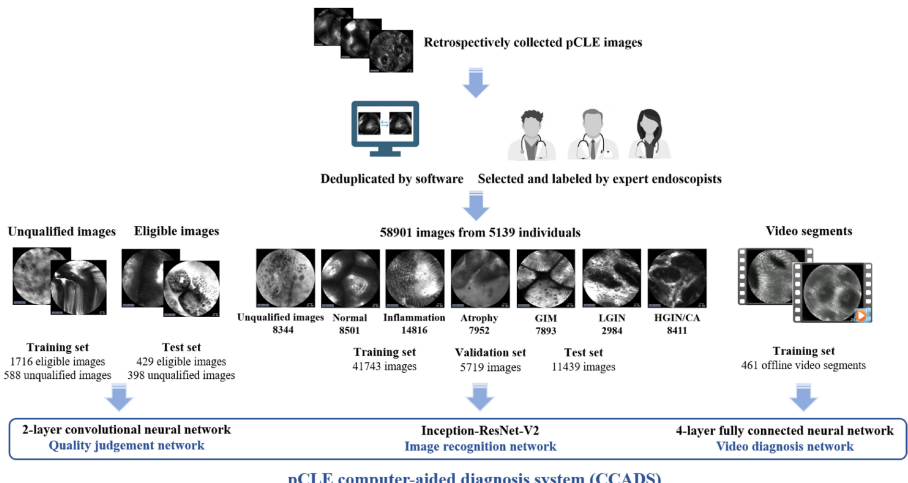
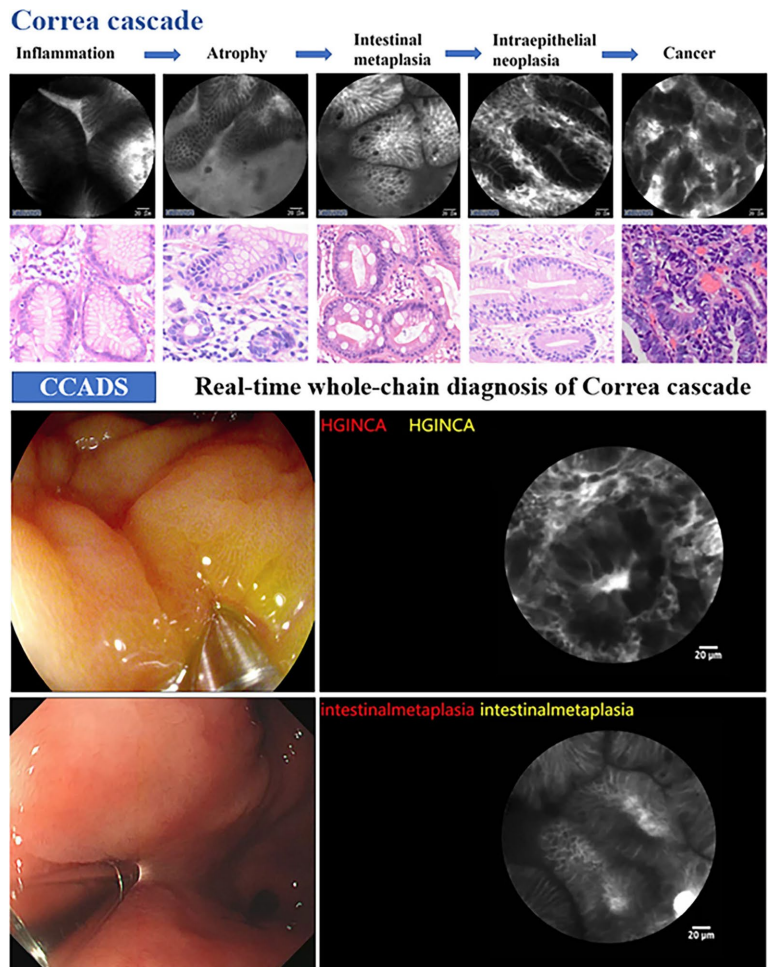
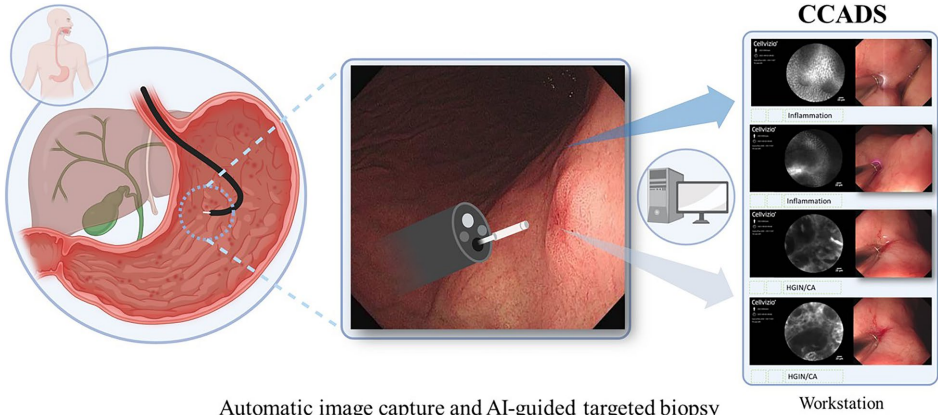
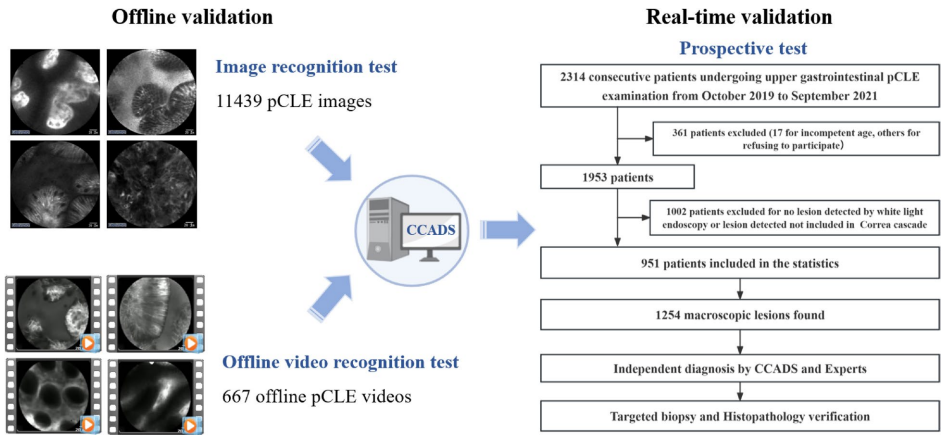
为解决胃镜检查中冗余活检增加患者负担和病理医生工作量、而探头式共聚焦激光内镜(pCLE)技术又因依赖专家经验难以推广的问题,研究人员开发了pCLE计算机辅助诊断系统(CCADS),通过深度学习实现胃癌Correa级联(炎症-萎缩-肠化生-异型增生-癌)的实时全链条诊断。前瞻性研究显示,CCADS对高级别上皮内瘤变/胃癌(HGIN/CA)的敏感度达98.44%,对 neoplasms(LGIN+HGIN/CA)的诊断敏感度显著高于专家(96.70% vs. 89.01%),可有效减少肿瘤漏诊,推动光学活检的临床应用。
生物通 版权所有