编辑推荐:
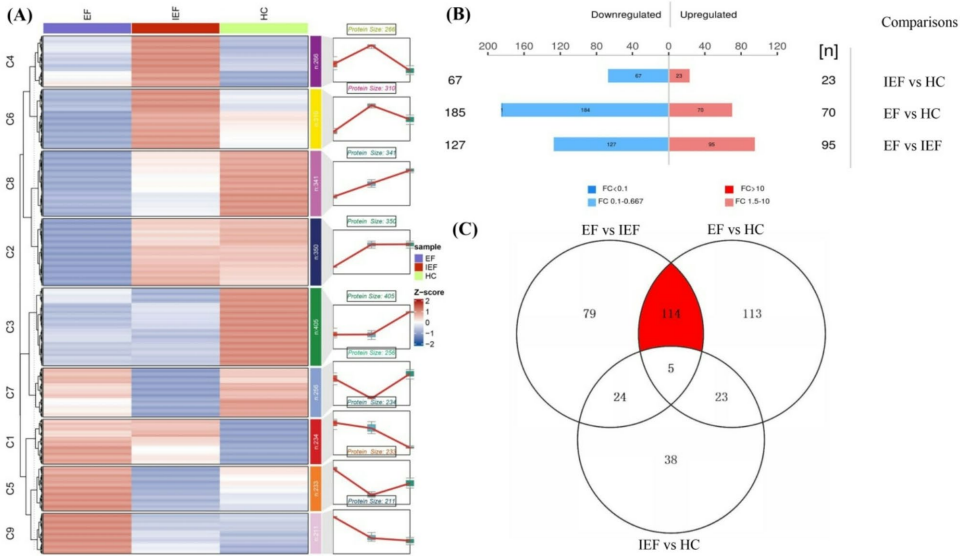
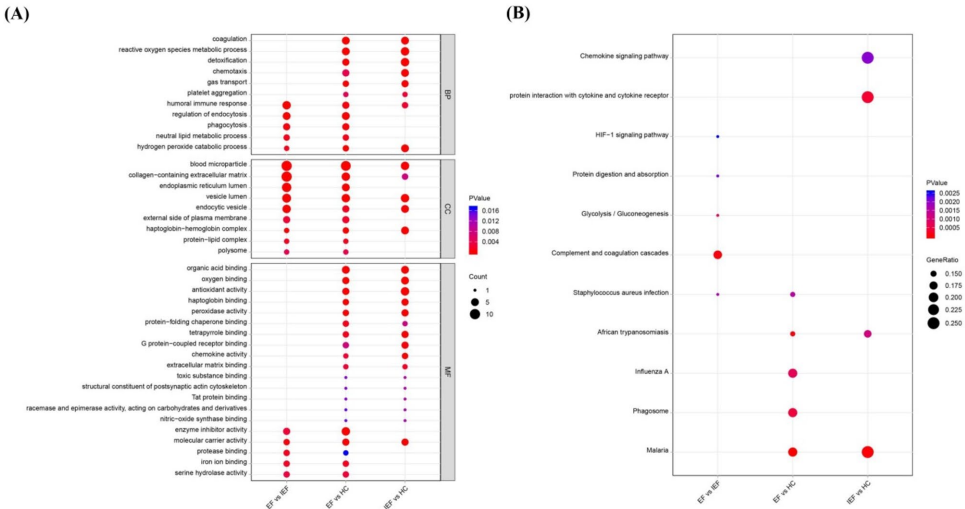
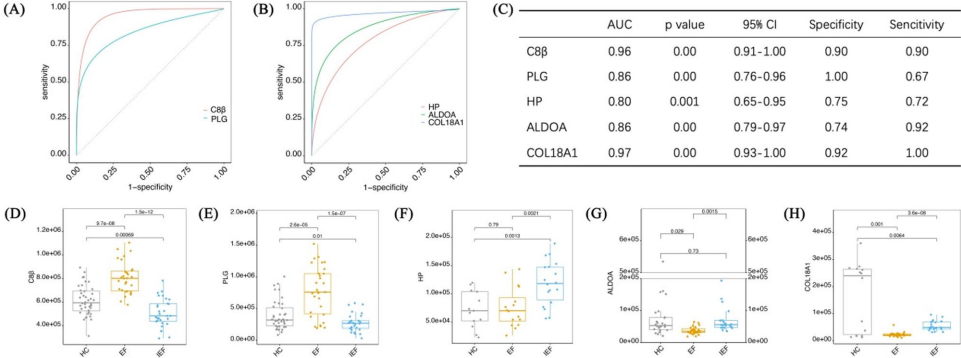
语 为解决婴儿癫痫性痉挛综合征(IESS)患者对促肾上腺皮质激素(ACTH)治疗反应差异的分子机制不明问题,研究人员开展了一项基于数据非依赖采集(DIA)质谱技术的血浆蛋白质组学研究。通过对比ACTH治疗有效(EF)与无效(IEF)患者,鉴定出114个差异表达蛋白(DEPs),其中补体成分8β(C8β)、纤溶酶原(PLG)、触珠蛋白(HP)、醛缩酶A(ALDOA)和胶原蛋白XVIIIα1(COL18A1)被验证为潜在预测标志物(AUC>0.8)。该研究为IESS的个体化治疗提供了新靶点,并首次揭示了免疫调节与代谢通路在ACTH疗效中的作用。
生物通 版权所有