编辑推荐:
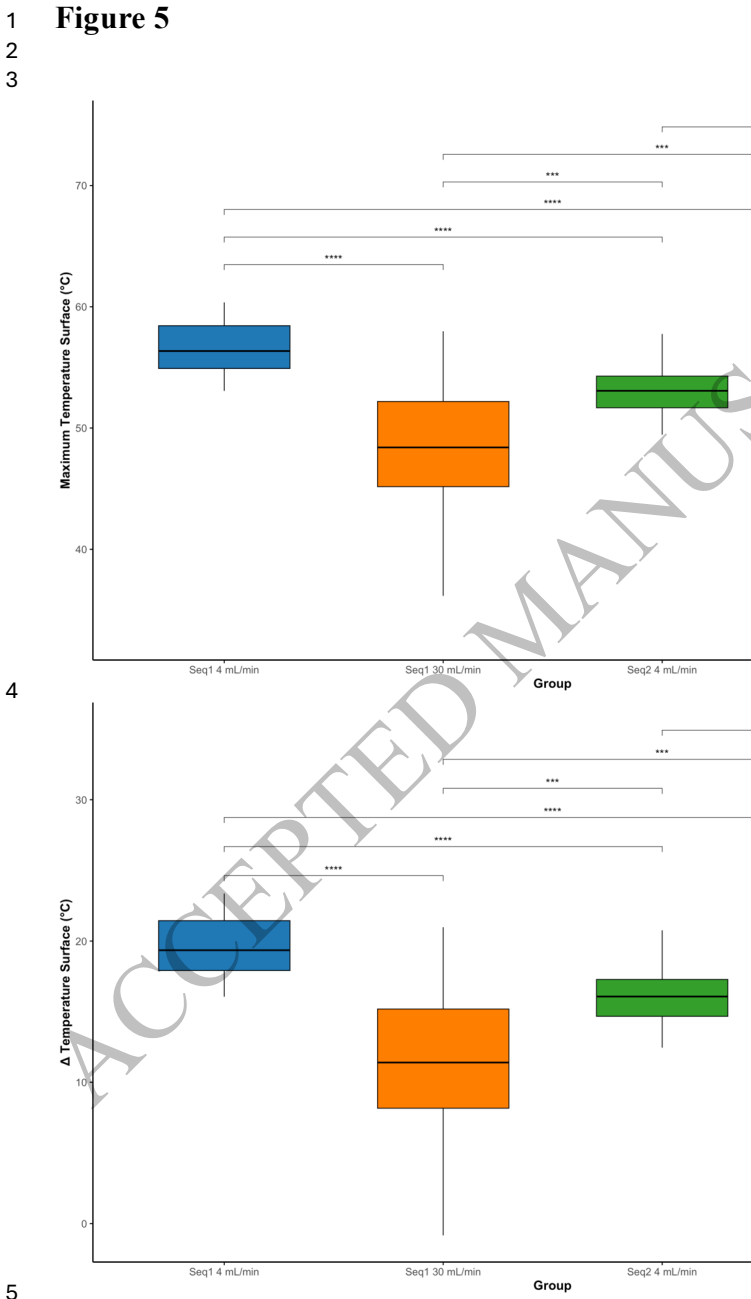
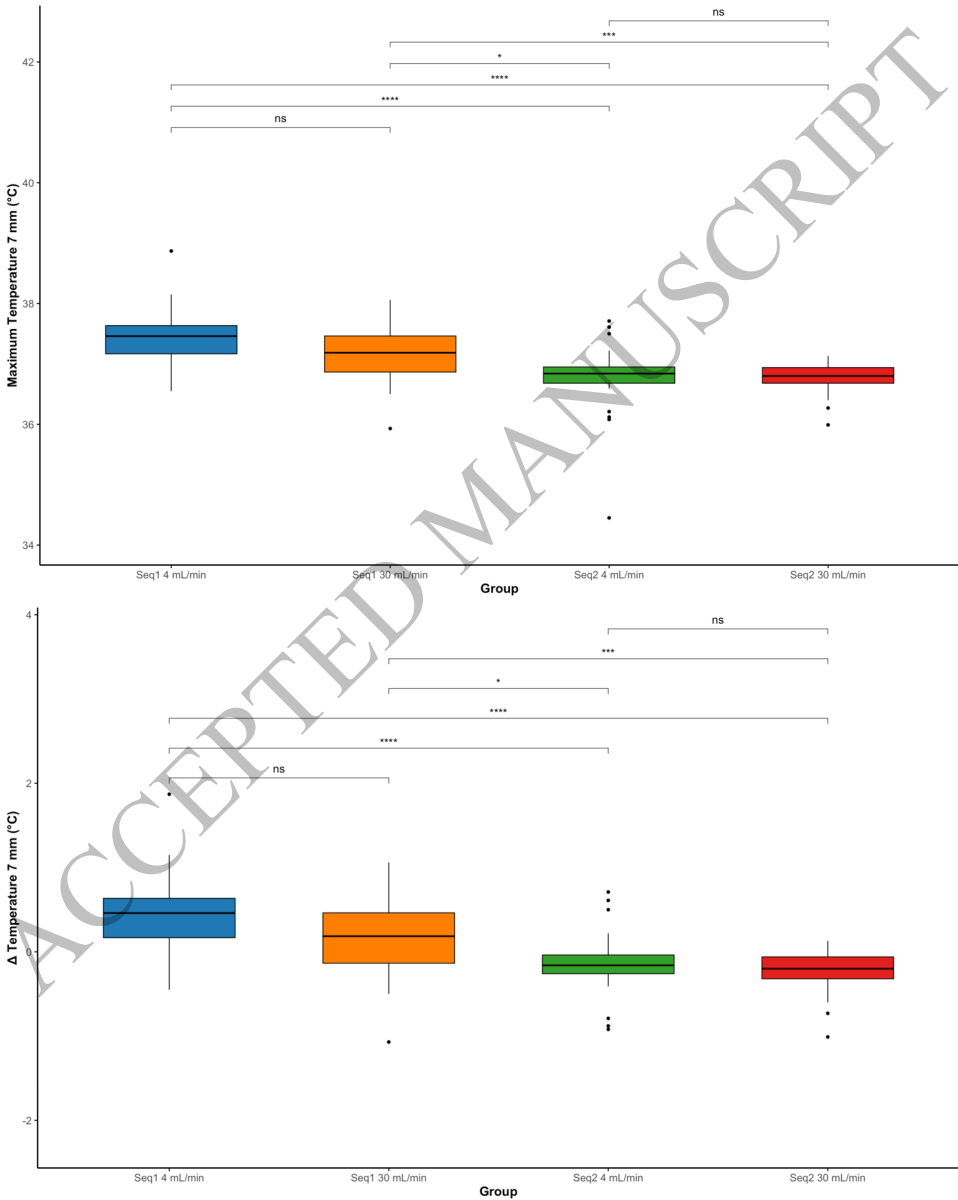
本研究针对脉冲电场消融(PFA)这一非热消融技术在临床应用中可能产生非忽视性热效应、增加血栓栓塞风险的问题,系统评估了可变环状圆形导管(VLCC)在不同波形配置(商业Sequence 1与实验性Sequence 2)和灌流速率(4 mL/min与30 mL/min)下的温度动力学特征。研究发现商业波形在低灌流时表面温度可达56.4°C,而优化波形结合高灌流可将温度显著降至40.8°C,证实通过波形优化和主动冷却可协同降低热负荷,为提升PFA安全性提供了重要循证依据。
生物通 版权所有