编辑推荐:
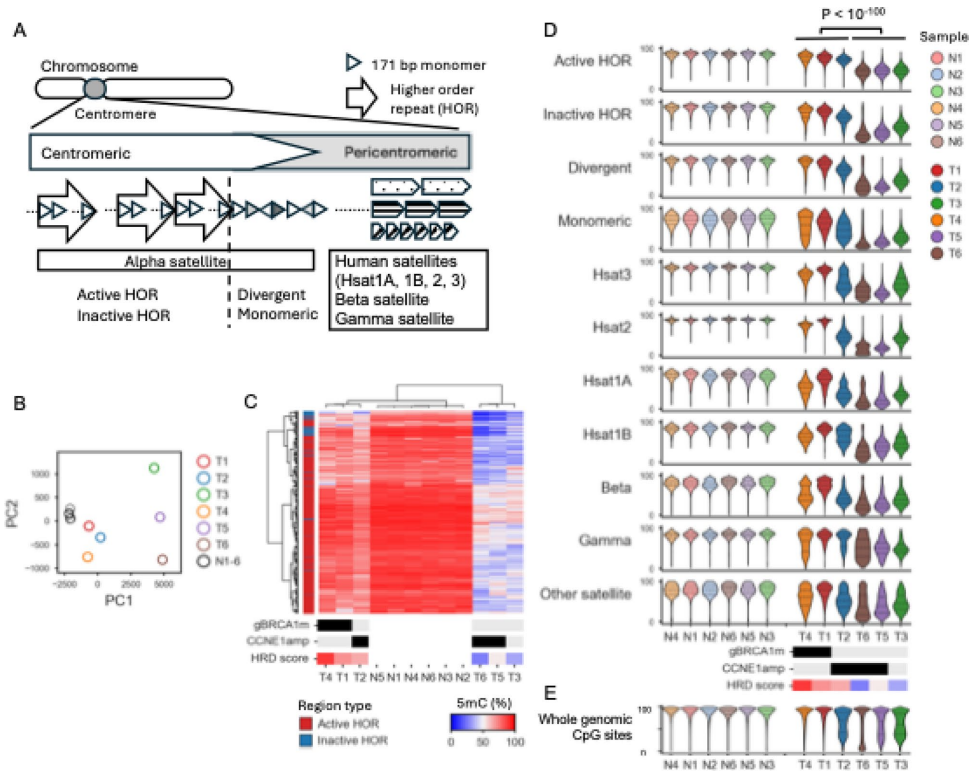
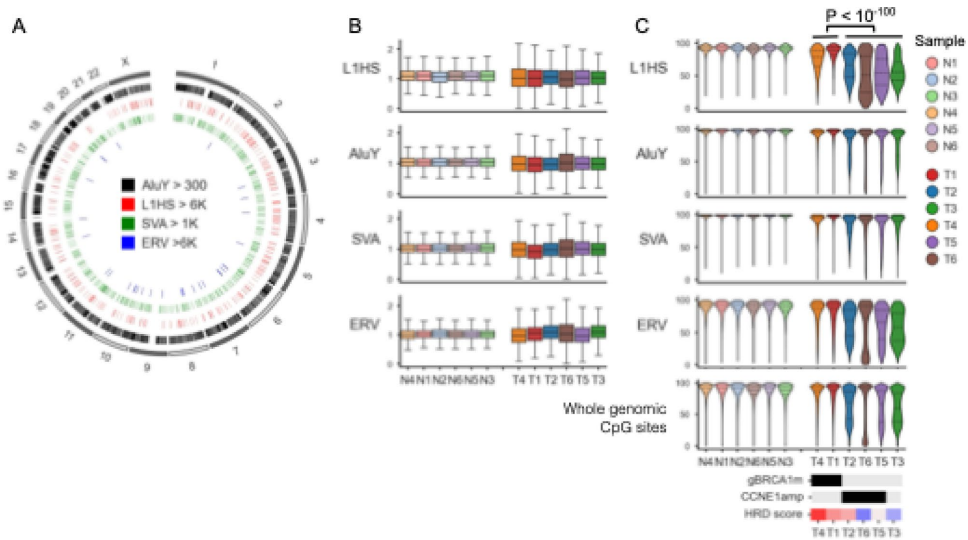
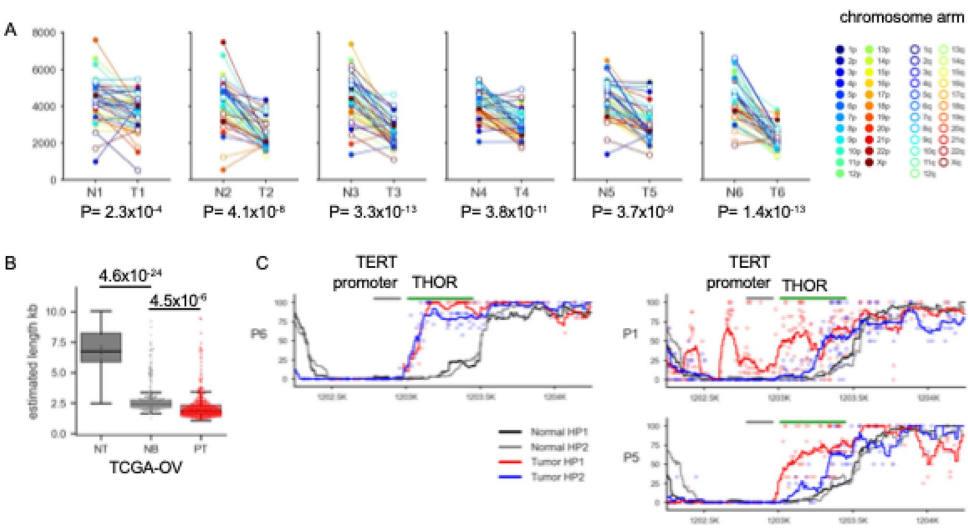
本研究针对高级别浆液性卵巢癌(HGSOC)中同源重组缺陷(HRD)对重复区域(如着丝粒和转座元件)的影响尚未明确的问题,采用牛津纳米孔长读长测序技术(LRS)结合T2T-CHM13参考基因组,首次在临床HGSOC样本中系统分析了着丝粒低甲基化、转座元件变异及端粒缩短等分子特征。结果发现HRD肿瘤与着丝粒特异性低甲基化模式显著相关,且LINE1/ERV元件的低甲基化程度与BRCA1突变状态相关,同时揭示了等位基因特异性TERT启动子超甲基化(THOR)可能作为端粒酶激活的新机制。该研究为HGSOC的分子分型提供了新视角,凸显了LRS在解析癌症重复基因组中的独特价值。
生物通 版权所有