编辑推荐:
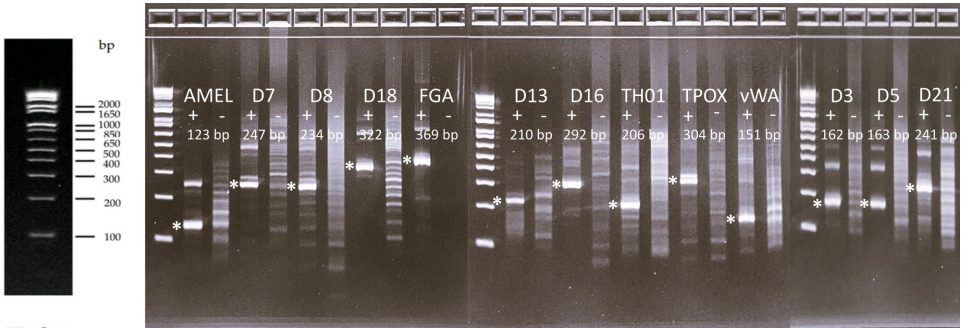
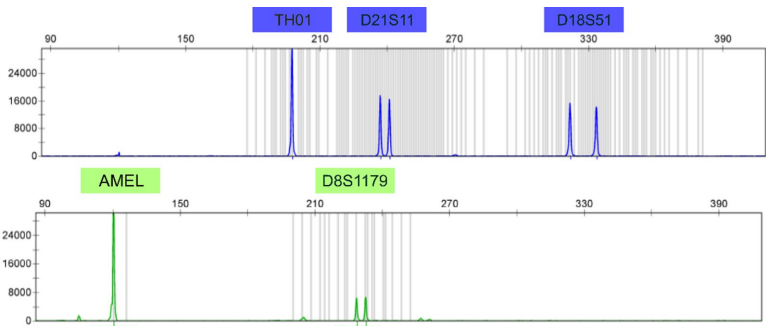
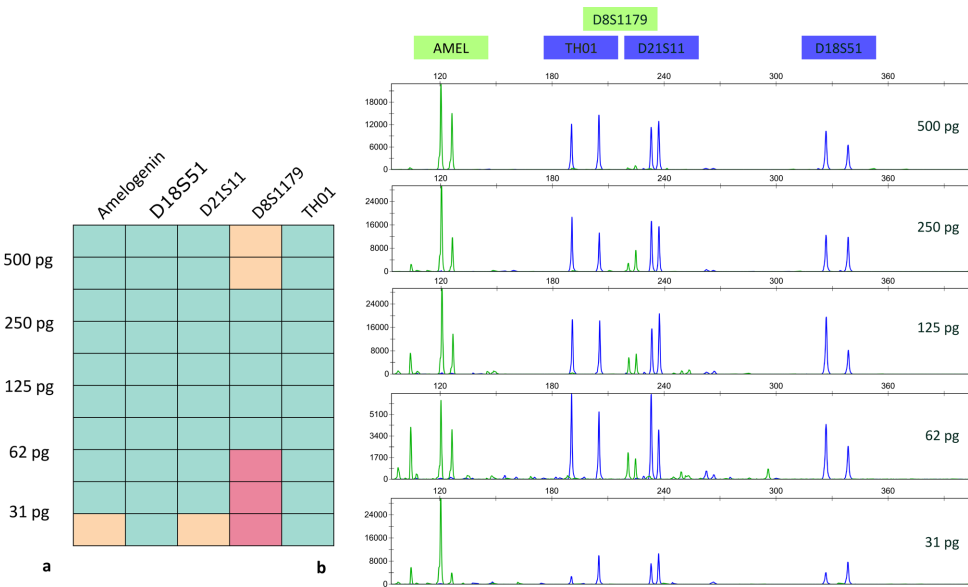
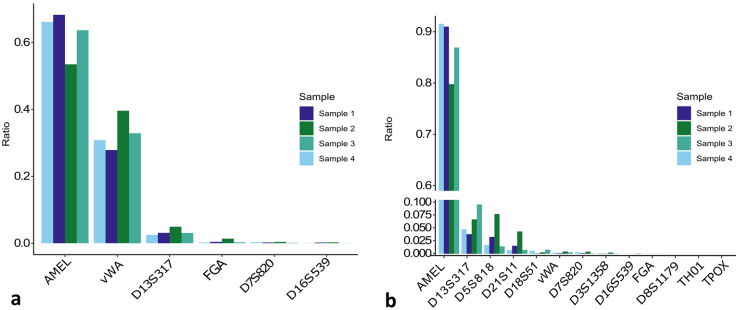
本研究针对法医DNA鉴定中对快速、低成本、便携式STR分型方法的需求,探索了利用重组酶聚合酶扩增(RPA)这一等温扩增技术替代传统PCR的可行性。研究人员成功使用RPA对CODIS系统的13个核心STR基因座进行了单重扩增,并通过毛细管电泳(CE)、Illumina和牛津纳米孔(ONT)测序验证了分型准确性,在1 ng DNA输入下获得完整正确的STR图谱,灵敏度达62 pg。尽管多重RPA扩增仍面临挑战,但此概念验证为开发便携式微流控STR分型设备及优化现有工作流程提供了新思路。
生物通 版权所有