编辑推荐:
这篇综述系统阐述了超声(US)技术在肿瘤诊疗中的多维度突破。从对比增强超声(CEUS)靶向血管标志物(如VEGFR2、PD-L1)的分子成像,到高强度聚焦超声(HIFU)热消融和声动力疗法(SDT)通过活性氧(ROS)介导的肿瘤杀伤,再到超声辅助药物递送系统(US-DDS)突破血脑屏障(BBB)和调控免疫微环境,全面展现了超声技术在精准肿瘤医学中的革新潜力。
超声凭借非侵入性、实时成像和高分辨率优势,已成为肿瘤早期筛查的关键工具。对比增强超声(CEUS)通过微泡(MBs)和纳米泡(NBs)靶向血管生物标志物,显著提升肿瘤可视化。例如,靶向VEGFR2的BR55造影剂在前列腺癌和肝癌中实现分子水平成像,而PD-L1靶向纳米泡可通过超声信号评估免疫检查点表达水平。多模态超声(MU)结合弹性成像和自动乳腺容积扫描(ABVS)等技术,与MRI/CT联用可将肝肿瘤诊断敏感性提升至97.85%。
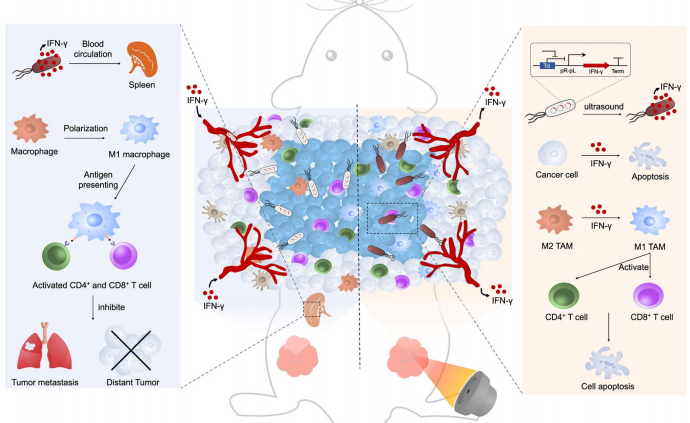
高强度聚焦超声(HIFU)通过局部升温至55°C以上诱导凝固性坏死,在前列腺癌治疗中实现90%肿瘤控制率。低强度聚焦超声(LIFU)联合声敏剂(如氮掺杂石墨烯量子点)产生ROS,通过PEX-p53通路触发肿瘤细胞凋亡,小鼠模型中肿瘤体积减少95%。创新性温度敏感工程菌(URB)在HIFU加热下分泌IFN-γ,激活M1巨噬细胞和CD8+T细胞,形成系统性抗肿瘤免疫记忆。
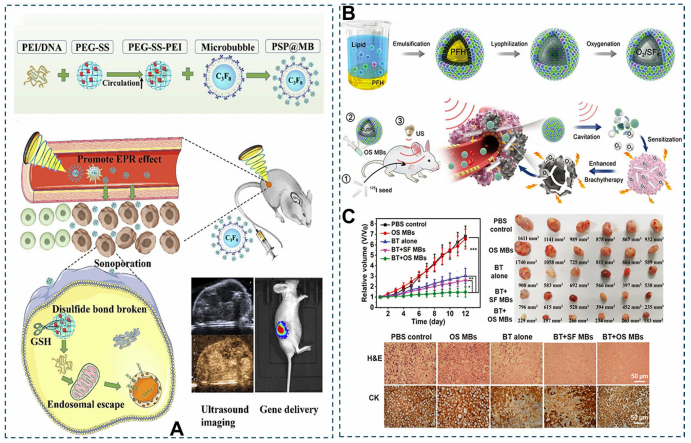
微泡/纳米泡的惯性空化效应可增强化疗药物穿透性,如紫杉醇负载微泡使胰腺癌模型药物递送效率提升3.2倍。氧载微泡(TPGS-SMS)通过超声触发释氧,将放疗组肿瘤体积增幅从337%降至41%。血脑屏障(BBB)开放技术联合鼻内给药,实现中枢神经系统靶向递送,24小时内屏障完整性可逆恢复。
沸腾组织切除术(BH)通过释放肿瘤抗原激活CD8+T细胞浸润,联合抗CD40抗体使黑色素瘤模型远端肿瘤消退。超声微泡携带PD-1抑制剂可提升肿瘤局部药物浓度,小鼠生存期显著延长。
尽管超声诊疗展现出巨大潜力,但纳米材料的长期生物相容性、声敏剂稳定性及深度组织穿透效率仍需优化。未来结合人工智能和穿戴式设备,有望实现程序化纳米机器人等突破性应用。
生物通 版权所有