编辑推荐:
本研究针对KRAS G12C突变型转移性结直肠癌(mCRC)患者对传统治疗耐药的关键临床问题,通过开放标签II期试验评估了新型KRAS G12C抑制剂Garsorasib(D-1553)单药及联合EGFR抗体西妥昔单抗的疗效。结果显示联合组客观缓解率(ORR)达45.2%,中位无进展生存期(PFS)7.5个月,显著优于单药组(ORR 19.2%,PFS 5.5个月),且安全性可控。该研究为亚洲人群占比最高(85.7%)的KRAS G12C靶向治疗提供了重要循证依据,发表于《Signal Transduction and Targeted Therapy》。
研究背景与科学问题
结直肠癌(CRC)是全球癌症死亡的第二大原因,其中KRAS突变约占40%,而KRAS G12C亚型虽仅占3%,却与极差的预后显著相关。传统抗EGFR治疗对此类患者无效,KRAS蛋白因缺乏结合口袋长期被视为"不可成药靶点"。2013年KRAS G12C变构结合位点的发现打破了这一僵局,但已获批的sotorasib和adagrasib在CRC中的单药疗效远逊于非小细胞肺癌(NSCLC),ORR仅9.7-29.1%,提示CRC存在独特的EGFR介导的MAPK通路反馈激活耐药机制。
中山大学肿瘤防治中心联合国际多中心团队开展了这项II期研究,旨在验证国产KRAS G12C抑制剂Garsorasib能否克服单药疗效瓶颈。临床前数据显示其可穿透血脑屏障并维持24小时靶点抑制,而联合西妥昔单抗可阻断EGFR驱动的耐药通路。研究结果发表于《Signal Transduction and Targeted Therapy》,为KRAS G12C突变mCRC提供了新的治疗选择。
关键技术方法
采用多中心、非随机、开放标签设计,纳入68例经治KRAS G12C突变mCRC患者(单药组26例,联合组42例)。单药组接受Garsorasib 600mg bid口服,联合组加用西妥昔单抗(首剂400mg/m2
,后续250mg/m2
/周)。主要终点为研究者评估的ORR(RECIST 1.1标准),次要终点包括DCR、PFS、OS和安全性(CTCAE 5.0标准)。
研究结果
疗效数据
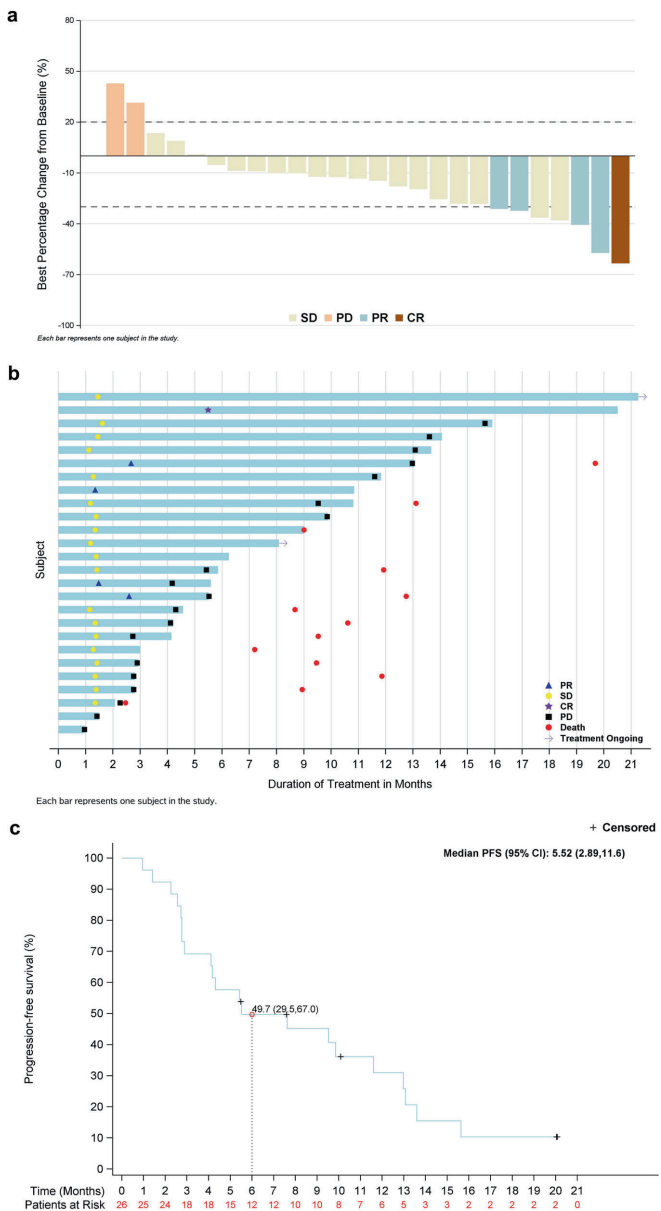
单药组ORR 19.2%(5/26,含1例CR),DCR 92.3%,中位PFS 5.5个月,OS 13.1个月。联合组ORR提升至45.2%(19/42),DCR 92.9%,中位PFS达7.5个月,OS未达到。亚组分析显示无论既往治疗线数、肿瘤部位,联合方案均显示优势。
安全性特征
单药组19.2%患者发生≥3级治疗相关不良事件(TRAE),主要为肝酶升高(ALT 11.5%,AST 7.7%);联合组≥3级TRAE发生率14.3%,以皮疹(4.8%)为主。值得注意的是,联合组未出现Garsorasib相关停药事件,且肝胆毒性发生率低于单药组。

结论与意义
该研究首次证实Garsorasib联合西妥昔单抗在KRAS G12C突变mCRC中具有协同作用:
研究局限性包括非随机设计和小样本量,但为后续III期试验奠定了坚实基础。目前Garsorasib联合方案已成为中国KRAS G12C突变mCRC患者最具潜力的精准治疗选择。
生物通 版权所有