编辑推荐:
这篇综述系统阐述了细胞衰老(Senescence)在癌症中的双重角色:既是抑癌机制(通过癌基因诱导衰老OIS和DNA损伤反应DDR),又是促癌因素(通过衰老相关分泌表型SASP和代谢重编程)。文章创新性地提出靶向衰老的治疗策略(如精准衰老清除剂Senolytics、衰老形态调节剂Senomorphics),并强调结合免疫治疗、代谢干预和表观遗传调节剂的联合疗法前景。
细胞衰老在癌症生物学中展现出令人着迷的双重性——既是守护者又是背叛者。这种不可逆的细胞周期停滞状态通过癌基因诱导衰老(OIS)和DNA损伤反应(DDR)途径筑起抗癌第一道防线,却又通过衰老相关分泌表型(SASP)和代谢重编程为肿瘤进展铺路。
抑癌机制方面,OIS通过激活p16INK4a/RB和p53/p21通路阻止癌前病变发展。DNA损伤时,ATM/ATR-CHK1/2-p53-p21级联反应触发衰老,而BRCA1缺失会削弱这种保护。短期SASP分泌IL-6、IL-8等因子招募NK细胞和T细胞清除衰老细胞,形成天然抗癌免疫。
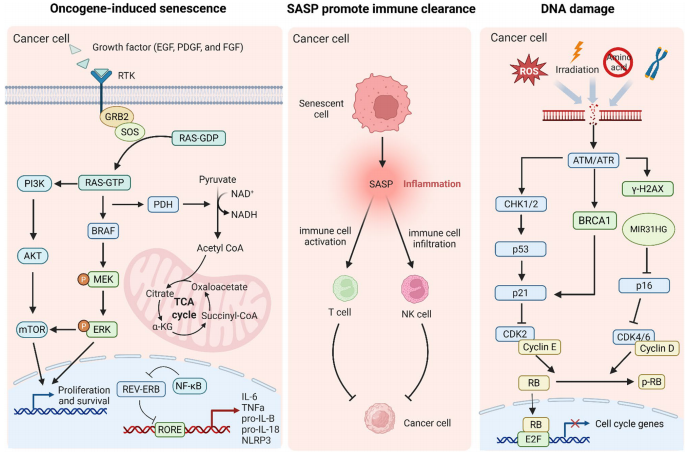
然而持续SASP通过cGAS-STING-NF-κB轴驱动慢性炎症,而ACSS2-PAICS轴调控嘌呤代谢加剧这一过程。代谢重编程中,线粒体功能障碍导致ROS爆发,Warburg效应增强乳酸分泌,营养竞争塑造免疫抑制微环境。免疫衰老表现为CD28-CD57+ T细胞累积和MDSCs扩增,通过IDO/犬尿氨酸/AhR通路抑制抗肿瘤免疫。
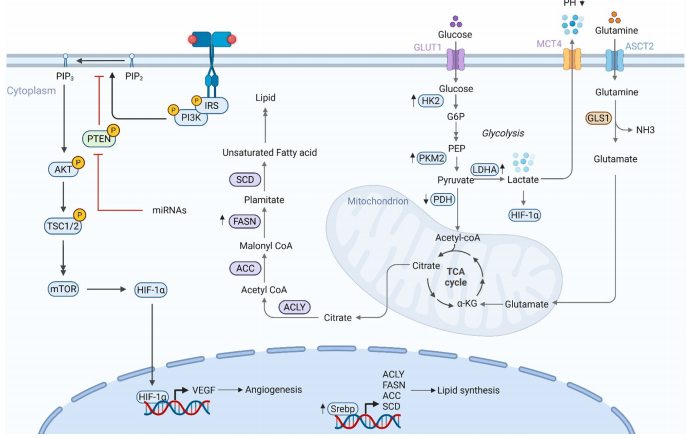
表观遗传调控构成另一维度:HDAC4降解导致H3K27乙酰化激活衰老程序,UHRF1诱导全基因组甲基化紊乱,lncRNA GAS5通过miRNA海绵作用调控衰老基因。这些变化在消化系统肿瘤中尤为显著,如CRC中USP11-p53轴和FGGY诱导的SAHF,GC中CBX4通过SUMO化稳定YAP1逃逸衰老。
创新疗法呈现多元化趋势:靶向衰老的"精准爆破"策略包括mGL392纳米颗粒递送达沙替尼,DR5-CNV/DOX选择性清除衰老细胞;代谢干预如精氨酸酶剥夺ASS1缺陷型肿瘤,烟酰胺单核苷酸(NMN)恢复NAD+水平;表观遗传调节剂5-氮杂胞苷联合HDAC抑制剂重塑染色质景观。
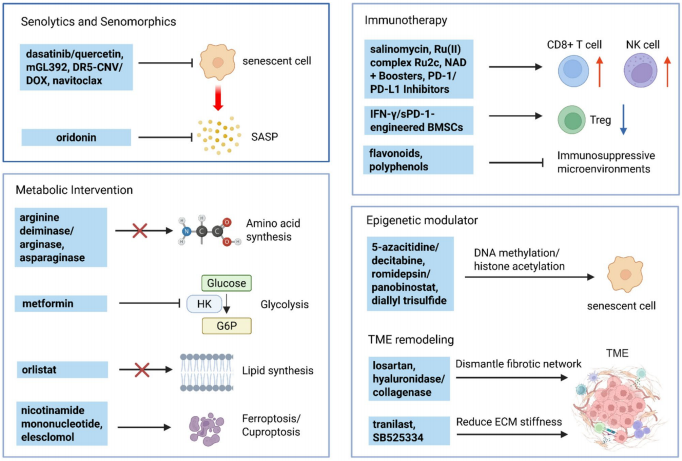
挑战与机遇并存:单细胞多组学揭示衰老异质性,CAV1+衰老细胞促进转移而MDH1+亚群影响药物敏感性;微生物组工程通过短链脂肪酸调节系统衰老;但衰老生物标志物的组织特异性、药物递送障碍和SASP的双向作用仍需突破。未来需开发时空特异性调控策略,平衡衰老的抑癌与促癌两面性。
生物通 版权所有